Комбинированная глаукома – это заболевание, характеризующееся повышением внутриглазного давления, которое может быть вызвано как открытоугольной, так и закрытоугольной формами глаукомы. Это состояние требует комплексного подхода к диагностике и лечению, чтобы предотвратить прогрессирование и сохранить зрение.
Лечение комбинированной глаукомы обычно включает использование глазных капель для снижения давления, которые могут содержать β-блокаторы, простагландины или ингибиторы карбоангидразы. В некоторых случаях может потребоваться хирургическое вмешательство для более эффективного контроля давления внутри глаза. Важно, чтобы лечение назначалось врачом с учетом индивидуальных особенностей пациента.
- Определение: Комбинированная глаукома — это заболевание, при котором наблюдается повышение внутриглазного давления, часто сопровождающееся повреждением зрительного нерва.
- Причины: Включает наследственные факторы, возрастные изменения, травмы глаза и другие заболевания глаз.
- Симптомы: Могут включать расширение зрачка, ухудшение ночного зрения и появление цветных кругов вокруг источников света.
- Методы лечения: Включают медикаментозную терапию, лазерные процедуры и хирургическое вмешательство в тяжелых случаях.
- Препараты: Чаще всего назначают препараты, снижающие внутриглазное давление, такие как бета-блокаторы, простагландины и альфа-адреномиметики.
- Важно: Регулярные проверки у офтальмолога необходимы для контроля состояния и предотвращения осложнений.
Вторичная глаукома и ее лечение
Глаукома представляет собой серьезное заболевание глаз, приводящее к атрофии зрительного нерва и клеток сетчатки, что в свою очередь ведет к необратимой утрате зрения. Она получает статус вторичной, если возникает в результате других заболеваний или травм. Вторичная глаукома может вызвать тяжелые последствия, включая полную слепоту, и часто встречается у людей в возрасте трудоспособности. Поэтому ключевую роль играют ранняя диагностика и эффективное лечение, что делает эту проблему особенно актуальной с социальной и медицинской точки зрения.
Заболевание имеет множество причин. Вторичную глаукому можно разделить на различные виды в зависимости от источника ее возникновения:
- Воспалительная – возникает вследствие увеита и воспалительных процессов в сосудистой системе глаза, вызывая образование экссудата, который затрудняет отток внутриглазной жидкости. При хроническом воспалении формируются спайки, закрывающие дренажную систему.
- Факогенная – связана с патологиями хрусталика, включая его смещение, изменение формы или целостности.
- Сосудистая – обусловлена прорастанием сосудов из радужки в угол передней камеры и повышением давления в сосудах эписклеры.
- Травматическая – развивается вследствие травм глаза, где повышение внутриглазного давления может проявиться даже через продолжительное время после повреждения.
- Послеоперационная – проявляется как осложнение после операций по поводу катаракты, пересадки роговицы или отслойки сетчатки. Обычно давление в глазу восстанавливается со временем, однако при наличии сопутствующих заболеваний может возникнуть стойкая вторичная глаукома.
- Дистрофическая – связана с нарушениями кровоснабжения тканей глаза, такими как синдром Фукса, отслойка сетчатки и дистрофия радужки.
- Неопластическая – возникает из-за роста опухоли, которая блокирует путь для оттока внутриглазной жидкости.
Диагностика вторичной глаукомы
Для диагностики заболевания и выявления его причин полезно провести комплексное исследование органа зрения. Это исследование включает как традиционные диагностические методы, так и современные высокотехнологичные процедуры. Каждому пациенту выполняются:
- измерение остроты зрения;
- оценка внутриглазного давления;
- периметрия;
- анализ состояния диска зрительного нерва;
- биомикроскопия;
- гониоскопия.
По показаниям пациентам назначается компьютерная или магнитно-резонансная томография, оптическая когерентная томография. В клинике профессора Трубилина специалисты индивидуально подходят к каждому пациенту, помогая ему обнаружить сопутствующие патологии, которые ухудшают течение глаукомы.
Комбинированная глаукома представляет собой особую форму глаукомы, при которой сочетаются два типа этого заболевания: первичная открытоугольная и закрытоугольная глаукома. Это состояние характеризуется повышением внутриглазного давления и повреждением зрительного нерва, что может привести к потере зрения. Важно понимать, что комбинированная глаукома требует комплексного подхода к диагностики и лечению, поскольку симптомы и протекание заболевания могут варьироваться у разных пациентов.
Лечение комбинированной глаукомы зависит от стадии заболевания и индивидуальных особенностей пациента. В большинстве случаев терапия начинается с назначения медикаментов, направленных на снижение intraocular pressure. Наиболее распространенными являются бета-блокаторы, простагландины, альфа-агонисты и ингибиторы карбоан гидразы. Эти препараты помогают снизить выработку водянистой влаги или увеличить её отток, что в свою очередь способствует нормализации внутриглазного давления.
В случае, если медикаментозное лечение не приводит к необходимым результатам, может потребоваться хирургическое вмешательство. Существуют различные хирургические методы, такие как лазерная терапия и традиционные операции, которые помогают создать новые пути для оттока водянистой влаги, тем самым уменьшая внутричерепное давление. Важно, чтобы лечение комбинированной глаукомы проводилось под строгим наблюдением офтальмолога, который сможет скорректировать терапию в зависимости от динамики заболевания и состояния пациента.
Комбинированный метод лазерного лечения первичной узкоугольной (смешанной) глаукомы
В последние десятилетия было достигнуто значительное развитие в профилактике и лечении первичной глаукомы, а В изучении ее этиопатогенеза. Тем не менее, глаукома по-прежнему занимает ведущее место среди причин необратимой слепоты и инвалидности [2, 8], что оправдывает повышенный интерес специалистов к этой проблеме.
Среди основных типов первичной глакомы выделяют открытоугольную и закрытоугольную формы, а также особую – «смешанную» (комбинированную) глаукому [10]. Эта форма сочетает в себе признаки обеих типов глаукомы в одном глазу [4, 5, 10, 14]. Упрощенно, основные механизмы смешанной глаукомы можно представить следующим образом: относительный (функциональный) зрачковый блок – узкий профиль угла передней камеры (УПК) – разрушение интрамуральных путей оттока камерной жидкости (трабекулы и интрасклеральные коллекторы).
Поэтому лечение пациентов смешанной глаукомой имеет, как правило, комбинированный характер. Действие всех лечебных манипуляций (вмешательств) должно быть направлено на устранение, коррекцию комплекса тех причин, которые привели к повышению внутриглазного давления (ВГД), и восстановление функций дренажного аппарата глаза.
Основным принципом терапии первичной открытоугольной глаукомы (ПОУГ) служит нормализация уровня офтальмотонуса и предотвращение дальнейшего ухудшения глакоматозной оптиконейропатии. В современной клинической практике выделяют три подхода для достижения этих целей: медикаментозное лечение, лазерные процедуры и хирургические вмешательства. Лазерные методы лечения глаукомы становятся все более популярными благодаря своей патогенетической цели и малой инвазивности, обеспечивая нормализацию внутриглазного давления минимальными рисками осложнений.
Вопрос лечения пациентов с узкоугольной (смешанной) глаукомой остается актуальным и в настоящее время. Поскольку традиционные лазерные вмешательства, такие как трабекулопластика, становятся невозможными из-за узкости или частичного закрытия угла, возникает необходимость в разработке особых подходов.
Лазерное лечение пациентов со смешанной глаукомой требует использования разнообразных вмешательств, учитывающих как причины закрытоугольной (иридэктомия, гониопластика), так и открытоугольной глаукомы (трабекулопунктура, трабекулоспазис, трабекулопластика). Целями комбинированных лазерных процедур являются устранение относительного зрачкового блока, открытие доступа к дренажной зоне УПК и улучшение дренажной функции трабекулярной сети.
Нередко лазерное лечение первичной узкоугольной (смешанной) глаукомы ограничивается только иридэктомией. Однако гипотензивный эффект после успешно выполненной лазерной иридэктомии (ЛИЭ) и открытый доступ к дренажной зоне УПК различен, во многом зависит от степени, характера деструктивных изменений в УПК и дренажной системе глаза [1, 6, 23]. При смешанной глаукоме нормализация ВГД после лазерной иридэктомии без применения гипотензивных средств достигается по данным различных исследований лишь в 20-33% случаев [23, 24].
При лечении закрытоугольной глаукомы применяется периферическая лазерная иридэктомия, а для открытоугольной – методы активации трабекулы. Однако в случаях узкоугольной (смешанной) глаукомы целесообразно их комбинирование. Мы предложили методику, которая включает выполнение лазерной иридэктомии в сочетании с селективной лазерной трабекулопластикой (СЛТ) [11]. СЛТ является эффективным и безопасным вмешательством, получившим широкое применение в мировой клинической практике для лечения ПОУГ. Одним из ключевых достоинств этого метода является целенаправленное воздействие на клетки трабекулярного аппарата, содержащие меланин, без повреждения самой структуры трабекулы [9, 12, 13, 15-20].
Изучить эффективность комбинированного метода лазерного лечения – сочетания лазерной иридэктомии с селективной лазерной трабекулопластикой – у пациентов с первичной узкоугольной (смешанной) глаукомой.
Материалы и методы
В исследование были включены 72 пациента (72 глаза) с начальной (I) стадией первичной узкоугольной (смешанной) глаукомы. Возраст пациентов: от 58 до 82 лет (средний возраст – 65,1±6,56 года). Среди пациентов было 45 женщин и 27 мужчин.
Наблюдение за пациентами длилось до 4-х лет после проведения лазерного лечения.
Всем пациентам до и после лазерного лечения исследовали остроту зрения, поле зрения, проводили биомикроскопию, офтальмоскопию, гониоскопию, тонометрию, тонографию (тонограф ТНЦ 100), оптическую когерентную томографию (ОКТ) переднего отрезка глаза (Visante OCT, Carl Zeiss Meditec Inc., США), компьютерную периметрию по программе 30-2 на периметре «Humphrey» фирмы Carl Zeiss Meditec Inc. (Германия); площадь нейроретинального пояска и экскавации диска зрительного нерва оценивались методом HRT на ретинальном томографе HRT III Heidelberg Engineering (Германия).
У всех участников исследования был узкий угол передней камеры, с различной выраженностью в разных сегментах. Пигментация дренажной зоны оценивалась на уровнях 2-3 по классификации А. П. Нестерова.
Уровень ВГД (Р0) до лечения был в среднем равен 24,47±1,85 мм рт. ст. Среднее количество используемых пациентами гипотензивных средств до лазерной операции – 2,2±0,4.
Средняя острота зрения до начала лечения составила 0,718 ± 0,051.
Лазерная иридэктомия и СЛТ выполнялись на лазерной установке Tango фирмы Laserex (Австралия). Операции проводились под местной эпибульбарной анестезией 0,5% раствором проксиметакаина. Для достижения миоза пациентам проводили инстилляцию «Фотила».
На первом этапе всем пациентам проводилась лазерная иридэктомия в верхнем сегменте (с 11 до 1 часа) по стандартной методике. Энергия в импульсе колебалась от 2,2 до 2,6 мДж, количество импульсов было от 4 до 7.
Вторым этапом – непосредственно сразу после иридэктомии – проводилась СЛТ, к выполнению которой не было препятствий, так как УПК приобретал необходимую ширину для ее выполнения. На глаз устанавливали контактную линзу Гольдмана и осуществляли СЛТ по стандартной технологии: в нижней полуокружности УПК (1800) наносили 50-70 лазерных аппликаций на зону трабекулы (энергия импульса варьировала от 0,5 до 1, мДж).
Статистическая обработка полученных данных включала расчет среднего арифметического (М) и стандартного отклонения (σ). Для сравнения средних значений использовали t-критерий Стьюдента.
Результаты и обсуждение
Все процедуры проведены без осложнений. В раннем послеоперационном периоде пациентам назначались нестероидные противовоспалительные препараты в каплях в течение одной недели.
В первые сутки после лазерного лечения реактивный подъем ВГД, но не более чем на 3-4 мм рт. ст., был отмечен на 7 глазах из 72 (9,7%). Нормализация офтальмотонуса была достигнута в течение 1-2 дней назначением дополнительной гипотензивной терапии с последующим снижением ее интенсивности.
Процент послеоперационных гипертензий, отмеченных у обследуемых, был сопоставим с данными другой литературы по результатам СЛТ [15-20]. Другие осложнения, такие как воспалительные или геморрагические, не наблюдались.
Незначительное количество осложнений подтверждает безопасность и малую инвазивность предложенного метода лечения, которая обусловлена точной локальной направленностью лазерного воздействия.
У всех пациентов было достигнуто расширение УПК, что подтверждалось при проведении гониоскопии и данными ОСТ Visante (табл. 1).
При гониоскопии у всех пациентов в послеоперационном периоде (через 1-6 мес.) определялось «просветление» в зоне воздействия СЛТ (значительное снижение степени пигментации трабекулы).
Состояние гидродинамики глаза до и после комбинированного лазерного лечения у участников исследования представлено в табл. 2.
Данные тонографии свидетельствуют о том, что нормализация офтальмотонуса у обследуемых больных отмечается на фоне повышения (усиления) оттока камерной влаги через дренажный аппарат глаза, это подтверждается повышением значений коэффициента легкости оттока внутриглазной жидкости (С) в раннем и отдаленном послеоперационном периоде.
Ранее многие ученые отмечали недостаточный уровень снижения ВГД после лазерной иридэктомии.
Ерескин Н. Н. (1991) отметил снижение ВГД после лазерной иридэктомии в среднем на 5,2 мм рт. ст. и лишь в 31% случаев у пациентов с начальной стадией смешанной (узкоугольной) глаукомы. Автор особо подчеркнул, что исходный уровень ВГД у пациентов до лазерного лечения был лишь незначительно выше нормы [5].
Даниленко О. В., Большунов А. В. и коллеги (2014) в течение месяца после проведенной иридэктомии зафиксировали снижение ВГД в среднем на 3,29 мм рт. ст. [3].
Золотарёв А. В. и соавт. (2017) в результате проведенных исследований пришли к выводу, что выполнение лазерной иридотомии при первичной смешанной глаукоме эффективно лишь у 9,7% пациентов [7].
Кратковременность эффекта снижения давления объясняется несколькими патогенетическими механизмами блокировки УПК при узкоугольной и закрытоугольной глаукоме [21, 22].
Проведенное нами комбинированное лазерное лечение обладает взаимодополняющим действием на гидродинамику глаза за счет расширения УПК после лазерной иридэктомии и улучшения трабекулярного оттока камерной влаги после СЛТ. В отдаленном послеоперационном периоде нормализация ВГД у обследуемых пациентов была достигнута в 87,5% случаев (на 63 глазах из 72).
После 6 месяцев наблюдения было отмечено повышение ВГД у 1 пациента (1 глаз), через 12 месяцев – у 3 пациентов (3 глаза), а через 2 года и позже – у 6 пациентов (6 глаз). Всем этим пациентам была выполнена повторная СЛТ, что позволило нормализовать офтальмотонус. Среднее количество препаратов для понижения давления у обследуемых снизилось с 2,2 ± 0,4 до 1,02 ± 0,1.
В течение всего периода наблюдения состояние зрительных функций оставалось стабильным у большинства пациентов.
Острота зрения осталась без изменений у 80,5% пациентов (58 из 72 глаз). Снижение остроты зрения на 0,12 ± 0,08 было зарегистрировано у 14 пациентов (14 глаз) и объяснялось прогрессированием катаракты, существовавшей до лазерного вмешательства.
По данным компьютерной периметрии отрицательная динамика (расширение слепого пятна, увеличение количества абсолютных скотом в центральном поле зрения) была отмечена у 6 пациентов (6 глаз из 72 – 8,3%).
Границы периферического поля зрения остались стабильными у 96% пациентов (69 из 72 глаз). Легкое сужение периферического поля зрения на 5-10 градусов наблюдалось у 3 глаз (4% случаев): одно из них – через 2 года, два – через 3 года.
По данным HRT (табл. 3) отрицательная динамика в виде уменьшения объема неврального ободка, увеличения площади экскавации диска зрительного нерва была отмечена в 7% случаев (5 глаз из 72).
Стабилизация зрительных функций, полученных из периметрии и показатели состояния зрительного нерва (по данным HRT) подтверждают благоприятный характер протекания глакоматозного процесса у большинства обследованных.
Предложенный метод комбинированного лазерного лечения позволяет достигнуть нормализации ВГД за счет расширения УПК после ЛИЭ с последующей активацией трабекулы методом СЛТ у 87,5% пациентов.
Нормализация офтальмотонуса и стабилизация зрительных функций, а также показатели состояния зрительного нерва у большинства пациентов в отдаленном послеоперационном периоде подтверждают эффективность предложенной методики лечения начальной стадией первичной узкоугольной (смешанной) глаукомы. Одновременное проведение лазерной иридэктомии и СЛТ является безопасным подходом и значительно сокращает длительность лечения и восстановительный период для пациентов.
Страница источника: 30-35
Глаукома: определение болезни
Глаукома представляет собой общее наименование группы заболеваний офтальмологического характера, при которых наблюдается постоянное или временное увеличение внутриглазного давления (ВГД). Это состояние приводит к необратимым изменениям в сетчатке и поражению зрительного нерва, что может вызвать нарушения зрения, вплоть до полной слепоты.
Термин «глаукома» (от греч. glaukos — «водянистый синий») впервые был упомянут в трудах Гиппократа около 400 года до нашей эры. Так он называл глазную болезнь, приводящую к слепоте. Как стало известно позднее, знаменитый целитель не видел разницы между глаукомой и катарактой, поэтому объединял их в одно заболевание. Название glaukos болезнь получила из-за того, что роговица глаза на поздних стадиях может приобретать мутно-голубоватый оттенок.
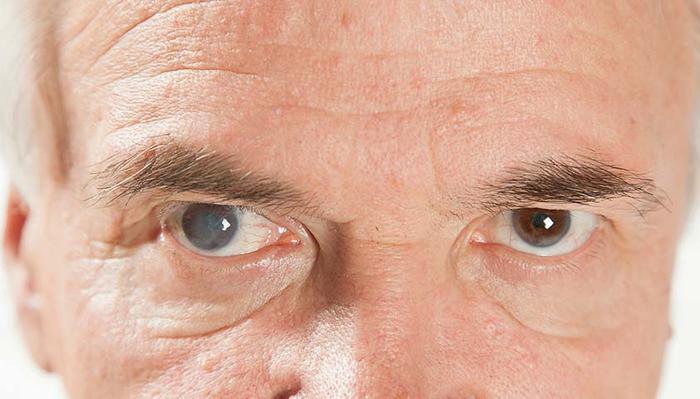
«Мутность» в глазах может указывать не только на наличие глаукомы, но и на другие офтальмологические заболевания, и лишь специалист может установить точный диагноз.
- H40.0 — подозрение на глаукому;
- H40.1 — первичная открытоугольная глаукома;
- H40.2 — первичная закрытоугольная глаукома;
- H40.3 — посттравматическая вторичная глаукома;
- H40.4 — вторичная глакома вследствие воспалительного заболевания глаза;
- H40.5 — вторичная глакома, вызванная другими глазными заболеваниями;
- H40.6 — вторичная глакома, ассоциированная с приёмом лекарств;
- H40.8 — другая форма глаукомы;
- H40.9 — глакома, не уточненная;
- Q15.0 — врождённая глакома.
Распространённость
Глаукома — грозное заболевание и главная причина необратимой слепоты. У многих пациентов патологические изменения затрагивают оба глаза. Каждый второй человек с глаукомой даже не подозревает о своей болезни.
Согласно данным Всемирной организации здравоохранения (ВОЗ), ежегодно фиксируется около 600 тысяч новых случаев слепоты, вызванной глаукомой. Общее число пациентов, страдающих этим заболеванием по всему миру, превысило 100 миллионов, из которых более 9 миллионов потеряли зрение на оба глаза.
Каждую минуту в мире от глаукомы слепнет один взрослый человек, а каждые 10 минут — один ребёнок.
Глаукома занимает лидирующую позицию среди причин инвалидности из-за болезней глаз почти во всех регионах России.
Капли от глаукомы

Глаукома Глаукома — большая группа глазных заболеваний, характеризующаяся постоянным или периодическим повышением внутриглазного давления выше приемлемого для данного человека уровня с последующим развитием типичных дефектов поля зрения, снижением остроты зрения и атрофией зрительного нерва. — распространенное нейродегенеративное заболевание, которое характеризуется устойчивым повышением внутриглазного давления.
Внутриглазное давление — давление жидкости внутри глаза. Это приводит к нарушению трофики внутренних структур глаза и со временем становится причиной атрофии зрительного нерва.
Зрительный нерв — вторая пара черепных нервов, по которым зрительные раздражения, воспринятые чувствительными клетками сетчатки, передаются в головной мозг. . Патология является причиной полной слепоты.
Слепота — медицинский термин, подразумевающий полное отсутствие зрения или его серьёзное повреждение. у 20 % больных, лишившихся зрения. Восстановить утраченную функцию глаза невозможно, однако это удается предотвратить. На начальных этапах болезни используются местные лекарственные средства в виде глазных капель от глаукомы. Они нормализуют ВГД Внутриглазное давление — давление жидкости внутри глаза. и препятствуют развитию ишемических изменений в глазном яблоке. Выбор конкретного препарата зависит от типа заболевания.
Препараты для снижения продукции внутриглазной жидкости
Используются при открытоугольной глаукоме Открытоугольная глаукома – она из двух форм развития глаукомы, при которой доступ к естественной дренажной системе открыт, но нарушены ее функции. , когда повышение внутриглазного давления обусловлено в первую очередь усилением продукции внутриглазной жидкости. Применяются в виде глазных капель, инстилляцию которых необходимо производить 2–3 раза в сутки. Назначаются препараты следующих групп:
- Стимуляторы α2-адренорецепторов. Примером служит клонидин, являющийся соединением, снижающим артериальное давление и стимулирующим α2-адренорецепторы. Эффект начинается через 30 минут, достигает максимума к 3 часам и сохраняется до 8 часов. Возможны побочные эффекты, включая сонливость и изменения пульса. Применение рекомендовано 2–4 раза в день в зависимости от степени болезни.
- Α- и β-адреноблокаторы. Эти препараты блокируют адреналиновые рецепторы (тимолол, некардиоселективный β-адреноблокатор). Применяется в форме глазных капель, обычно 1–2 раза в день. Начинает действовать через 20 минут, максимальная эффективность достигается через 2 часа и продолжается на протяжении суток. Не изменяет диаметр зрачка и кровообращение в передней камере. Побочные эффекты могут включать снижение давления и угнетение психических функций.
- Ингибиторы карбоангидразы. Этот класс препаратов подавляет активность карбоангидразы. Дорзоламид (торговое название Трусопт) снижает секрецию внутриглазной жидкости. Эффект проявляется через 2 часа и длится около 12 часов, может назначаться как самостоятельно, так и в сочетании с другими средствами, с минимальным количеством побочных эффектов.
Препараты, способствующие лучшему оттоку внутриглазной жидкости
Взаимодействуют со специфическими рецепторами, уменьшают сопротивление отводящих внутриглазную жидкость путей. Показаны в основном при закрытоугольной глаукоме Закрытоугольная глаукома – это резкое повышение внутриглазного давления вследствие блокирования путей оттока водянистой влаги. , спровоцированной нарушением увеосклерального оттока. Применяются средства таких групп, как:
- Холиномиметики, такие как пилокарпин, имитируют действие ацетилхолина, что влияет на работу органов, как при стимуляции холинэргических нервов. Основное назначение — улучшение оттока жидкости и снижение внутриглазного давления.
- Простагландины F2α. Эти вещества имитируют действие гормонов. Например, латанопрост применяется для снижения глаукомного давления и увеличивает увеосклеральный отток. Применяется в виде глазных капель одноразово в день, обычно вечером.
- Α- и β-стимуляторы, такие как дипивалил эпинефрина, могут улучшать отток и умеренно уменьшать продукцию жидкости. Чаще всего применяются 1–2 раза в день и могут использоваться у пациентов с сердечно-сосудистыми заболеваниями.
Лечение глаукомы начинается с применения одного препарата, но если его эффективность недостаточна, возможно добавление второго. Использование более двух средств одновременно не рекомендуется, однако комбинированные капли могут значительно улучшить лечение. Примеры таких комбинаций:
- «Фотил» — комбинированное средство (пилокарпин + тимолол).
- «Ксалаком» — помогает в лечении, сочетая латанопрост и тимолол;
- «Ганфорт» — содержит биматопрост и тимолол для снижения давления.
Как закапывать капли от глаукомы
Лекарственные средства следует закапывать через равные промежутки времени, как указано врачом. Перед инстилляцией обязательно нужно помыть руки, перевернуть флакон и запрокинуть голову. Нижнее веко следует аккуратно оттянуть и капли ввести в образовавшееся пространство. После процедуры глаз необходимо закрыть и немного помассировать для более быстрого всасывания. Излишки капель можно удалить с помощью чистой салфетки.
Обратите внимание: самостоятельное использование вышеописанных средств недопустимо. Большинство из них обладает серьезными побочными эффектами и может нанести вред вашему здоровью. Только использование медикаментов по назначению врача под соответствующим контролем делает лечение безопасным и эффективным.
Медикаментозное лечение глаукомы: обоснованные подходы к выбору терапии
Для сохранения зрительных функций у больных глаукомой используется гипотензивная терапия. В статье обсуждаются вопросы выбора целевого уровня давления, а также своевременной и рациональной интенсификации терапии для предотвращения прогрессирования заболевания. Дана характеристика препаратов первого выбора с позиций выраженности гипотензивного эффекта и препаратов для комбинированной терапии с точки зрения дополнительных благоприятных эффектов.
Для поддержания нормального уровня зрительных функций у пациентов с диагнозом глаукома применяют гипотензивную терапию. В данной статье анализируются аспекты определения целевого уровня внутриглазного давления (ВГД) и необходимость неотложной а также разумной коррекции терапии с целью предотвращения ухудшения состояния. Рассматриваются особенности препаратов первого выбора с точки зрения их гипотензивной активности, а Возможности комбинированной терапии, включая добавочные преимущества.
Несмотря на значительный прогресс в определении спектра заболеваний, объединенных понятием «глаукома», их патогенез до конца не ясен. Общий симптом этих заболеваний – уровень внутриглазного давления (ВГД), превышающий физиологически определенные нормы. Основная задача в лечении глаукомы – снизить офтальмотонус и сохранить зрительные функции в течение длительного времени.
В этой связи важно обсудить «реальную» норму ВГД. У 75% здоровых людей показатель нормального ВГД колеблется от 20 до 21 мм рт. ст. (по данным тонометрии Маклакова). Тем не менее, исследования как российских, так и зарубежных ученых показывают, что приблизительно 20% населения имеют значение ВГД ниже данного порога.
Еще один немаловажный аспект – колебания ВГД. Во всех руководствах по глаукоме [1, 2] сказано, что физиологические колебания составляют 3–5 мм рт. ст. (причем разница между значениями, определенными для правого и левого глаза, не должна превышать 2 мм рт. ст.). Однако это не всегда так. Ряд исследований, проведенных в разное время, а также самостоятельный суточный мониторинг ВГД позволяют усомниться в корректности подобных нормативов [3, 4].
Известно, что внутриглазное давление может колебаться в течение суток и в зависимости от времени года. Офтальмотонус варьирует в зависимости от положения тела, эмоционального состояния пациента и точности выполнения тонометрии. К сожалению, значению нормы ВГД зачастую уделяется недостаточно внимания. Однако при возникновении первых подозрений на глаукому важно учитывать этот параметр для назначения адекватного лечения. Нередко мы не имеем информации о индивидуальной норме офтальмотонуса и его колебаниях, что подчеркивает важность понимания безопасного уровня ВГД для пациента.
Наиболее масштабные потери ганглионарных (ганглиозных) клеток сетчатки при глаукоме происходят именно на начальной стадии, а уровень офтальмотонуса на ранних стадиях глаукомы играет роль индикатора заболевания [5]. Глаукома может прогрессировать и при низких значениях ВГД [6].
В целях изучения подходов к лечению глаукомы по инициативе Российского глаукомного общества было проведено несколько многопрофильных исследований как в России, так и в странах постсоветского пространства [7, 8, 9]. Полученные результаты ставят под сомнение устоявшиеся мнения о выборе начальной терапии глаукомы, где учитывать нужно не только уровень офтальмотонуса, но и стадию болезни.
Ранее выявленная зависимость длительности заболевания от продолжительности жизни пациентов говорит о том, что в среднем болезнь продолжается 11 лет при длительности жизни пациента около 64 лет (p > 0,05) [10]. Несколько авторов независимо друг от друга [10, 11, 12, 13, 14] установили среднюю продолжительность стадий глаукомы: начальная стадия длится 7,57 ± 0,57 года, развитая – 4,78 ± 0,34 и далеко зашедшая – 5,24 ± 0,78 года.
Наибольшее количество случаев прогрессирования заболевания наблюдается на начальных стадиях глаукомы. Замечено, что 48% пациентов перешли на более поздние стадии, из них 32% достигли развившейся стадии, а 16% – далеко зашедшей.
Таким образом, отчасти парадоксальные результаты этих исследований подтвердили «агрессивный» старт болезни и свидетельствовали о наиболее активном прогрессировании глаукомы в ее начальной стадии, то есть когда предполагаются лучший ответ на терапию и бóльшая толерантность зрительного нерва к повышенному офтальмотонусу. Почему, несмотря на терапию, заболевание максимально прогрессирует в начальной стадии? Можно ли определить вектор заболевания индивидуально? Достаточно ли активно начато лечение? Все ли повреждающие факторы учтены?
В современной офтальмологической практике используется разнообразие препаратов для снижения ВГД. Предпочтительнее применять монотерапию, но при необходимости можно комбинировать препараты с различными механизмами действия: чтобы уменьшить продукцию водянистой влаги и повысить отток внутриглазной жидкости.
Однако надо учитывать, что глаукома – непрерывный, хронически прогрессирующий патологический процесс и эффективность любых методов лечения постепенно снижается [11]. Серьезный прогноз заболевания требует не только адекватной индивидуально подобранной терапии на старте, но и ее своевременной коррекции в процессе наблюдения. Не стоит забывать и о такой важной составляющей успеха лечения, как взвешенное и аккуратное отношение к проводимой терапии со стороны пациента. А это возможно, только если пациент понимает необходимость постоянного лечения и наблюдения.
В офтальмологической практике эффективность гипотензивных средств обычно выражается в процентах. Считается, что снижение офтальмотонуса на 20–40% по сравнению с исходными показателями является достаточным для достижения целевого уровня давления. Уровень снижения часто зависит от стадии глаукомы, наличия сопутствующих заболеваний, наследственности и степени изменений в диске зрительного нерва (ДЗН). Целевой параметр может стать более строгим при прогрессировании заболевания [15]. Для продвинутых стадий глаукомы гипотензивный эффект должен составлять не менее 30–50% от исходного уровня ВГД. Рекомендации Национального руководства по глаукоме [1, 2] по снижению ВГД таковы:
- I* стадия – на 20% (21–23 мм рт. ст.);
- I**, II*, III* стадии – на 30% (17–20 мм рт. ст.);
- II**, III** стадии – на 35–40% (16 мм рт. ст.).
По данным опубликованных исследований [7, 8, 9], на фоне терапии удавалось достичь рекомендуемого уровня офтальмотонуса только в начальной стадии заболевания, в развитой стадии отмечались пограничные показатели, а в случае далеко зашедшей стадии фактический уровень ВГД существенно превышал целевые значения. Недостаточно низкий уровень ВГД у пациентов с продвинутыми стадиями глаукомы свидетельствует о необходимости более активной интенсификации терапии уже на начальной стадии заболевания. Вместе с тем, учитывая высокую долю пациентов, у которых заболевание переходит в следующую стадию даже при достижении достаточно низкого ВГД в начальной стадии, одно только снижение офтальмотонуса не является единственной достаточной целью фармакотерапии при глаукоме.
Таким образом, какой препарат следует использовать в начале терапии? Лидирующие лекарства с точки зрения гипотензивного действия – это препараты группы аналогов простагландинов, которые позволяют при рекомендованной схеме (один раз в день) добиться снижения офтальмотонуса в среднем на 30% от исходного уровня.
Из этой группы на российском рынке представлены препараты латанопрост (Ксалатан 0,005% и Глаупрост 0,005%) и травопрост (Траватан 0,004%). Их гипотензивная эффективность идентична. На практике аналоги простагландинов выбирают в среднем 12–15% докторов. В 66–67% случаев специалисты отдают предпочтение препаратам группы неселективных бета-блокаторов (в основном тимололу 0,25–0,5%-ному).
При использовании тимолола две раза в день наблюдается снижение офтальмотонуса на 25% от исходного уровня. У пациентов с развитыми и запущенными стадиями заболевания обычно нецелесообразно полагаться только на монотерапию, поэтому довольно скоро или сразу после начала лечения может возникнуть необходимость в комбинации с другими препаратами [16].
Какие комбинации эффективны? Какие препараты могут стать адекватной поддержкой сильным стартовым «лидерам» и когда?
Гипотензивная эффективность прочих групп препаратов (холиномиметические средства, селективные бета-адреноблокаторы, ингибиторы карбоангидразы и агонисты альфа-адренорецепторов) схожа и, как правило, значительно ниже, чем у препаратов первой линии – около 18–20% от исходного уровня. Однако препараты второго выбора предоставляют дополнительные положительные эффекты.
Добавление к препаратам первой линии селективных бета-адреноблокаторов (в некоторых случаях уже в начале терапии) оправданно в силу оказываемого ими дополнительного гипотензивного действия, а также благодаря нейропротекторным свойствам. Например, доказано, что бетаксолол 0,25–0,5%-ный (Бетофтан 0,5%) в большинстве случаев снижает ВГД в меньшей степени, чем неселективные бета-адреноблокаторы [17].
Благодаря увеличению скорости кровотока в крупных и мелких сосудах сетчатки и ДЗН препарат способствует улучшению глазного кровоснабжения [18, 19, 20, 21], что критически важно для пациентов с глаукомой, поскольку они часто испытывают нарушения микроциркуляции. Еще одним полезным свойством бетаксолола является его косвенное нейропротективное действие на сетчатку, вызванное блокировкой кальциевых каналов и связано с метаболизмом глутамата [22]. В связи с этим, при своевременном использовании комбинаций с нейропротекторным действием можно ожидать стабилизации состояния и даже незначительное восстановление повреждений при условии достижения безопасного уровня внутриглазного давления. Считаем, что лечение, нацеленное на снижение офтальмотонуса и нейропротекция, должно происходить одновременно на постоянной основе.
Другая группа препаратов для комбинированной гипотензивной терапии при глаукоме – ингибиторы карбоангидразы. В клинической практике применяются дорзоламид (Трусопт 2% и Дорзопт 2%) и бринзоламид (Азопт 1%). Они обладают схожими показателями эффективности в отношении снижения ВГД. Ингибиторы карбоангидразы блокируют этот фермент, их применение приводит к постепенному накопительному увеличению концентрации CO2 во всех тканях глаза, включая сетчатку. Как следствие, усиливается кровоток в сетчатке и зрительном нерве, улучшается кровоснабжение тканей глаза за счет вазодилатации, стабилизируются зрительные функции.
Для комбинированной терапии глаукомы рекомендован препарат из группы агонистов альфа-2-адренорецепторов – бримонидин (Альфаган Р 2%). Результаты доклинических исследований [23, 24, 25] отображают его способность предотвращать вторичную нейродегенерацию благодаря значительному повышению выживаемости ганглионарных клеток сетчатки в условиях ишемии. Клинические испытания бримонидина [26] на пациентах с нормотензивной глаукомой подтвердили уменьшение потерь полей зрения по сравнению с группой, принимающей неселективные бета-блокаторы, что объясняется противоишемическим действием данного препарата.
Как известно, структурные изменения нервных волокон сетчатки и зрительного нерва предшествуют изменениям зрительных функций (показатель повреждения зрительного нерва – ухудшение полей зрения). Отсутствие прогрессирования потери зрения при индивидуально и своевременно подобранной терапии, а также при достижении безопасного целевого уровня давления теоретически может являться показателем нейропротекторного действия препарата и фактически подтверждать если не полную стабилизацию, то по крайней мере значительное замедление скорости прогрессирования глаукомы. Таким образом, активный старт терапии, ее своевременная адекватная коррекция, подбор комбинаций препаратов, позволяющих не только дополнительно снижать внутриглазное давление, но и обеспечивать постоянную нейропротекцию, позволяют длительно сохранять зрительные функции у пациентов с глаукомой. Именно такая задача стоит сегодня перед офтальмологами.
Периодически при ПОУГ наблюдаются очень высокие значения ВГД
Боль не служит диагностическим признаком, так как ВГД постепенно возрастает.
Внимательные пациенты сами могут заметить области потери зрения.
Каков план действий для врача общей практики, чтобы не упустить начало заболевания? Во-первых, следует обязательно направлять пациента к офтальмологу, если данные оптометрических исследований создают подозрения на первичную открытоугольную глаукому (ПОУГ).
Во-вторых, целесообразно предлагать пациенту регулярно (раз в два года) проходить зрительные тесты и при этом просить офтальмолога целенаправленно искать признаки глаукомы. Этот совет особенно актуален в отношении людей с повышенным риском развития глаукомы, представителей афро-карибской национальности и при наличии глаукомы в семейном анамнезе.
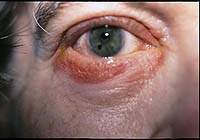 |
| Рисунок 3. Повышенная чувствительность может развиваться на основе любого компонента местных лекарственных средств, включая действующее начало и консерванты |
Кроме того, в-третьих, с учетом того, что научные и медицинские представления о ПОУГ со временем эволюционируют, пациенты с низким риском развития глаукомы могут быть исключены из стационарного учета, но им все же рекомендуется регулярное обследование у офтальмолога.
Лечение направлено на снижение ВГД до безопасного уровня. Как правило, к средствам первого ряда относятся местные β-блокаторы, такие как левобунолол или тимолол, при этом важно учесть, что их побочные эффекты не отличаются от побочного действия β-блокаторов, принимаемых внутрь.
В настоящее время предлагаются новые терапевтические средства, такие как α-агонисты (бримонидин и апраклонидин) и аналоги простагландина (латанопрост). Старые препараты, такие как пилокарпин и адреналин, не нашли широкой популярности.
Раньше считалось, что хирургическое вмешательство (трабекулотомия) необходимо только при отсутствии эффекта от консервативных методов, однако в ряде исследований описываются хорошие результаты операций, проведенных на ранних стадиях.
Глаукома нормального давления. У пациентов, у которых значения ВГД не превышали 21 мм рт. ст., но наблюдаются симптомы глаукоматозного ухудшения диска зрительного нерва и потеря полей зрения, диагностируется глаукома нормального или, как раньше говорили, низкого давления.
Однако значение 21 мм рт. ст. составляет не более 95% от ВГД в популяции и во многом является относительным ориентиром. В этом случае крайне необходим индивидуальный подход, ведь у одних людей обнаруживается сужение поля зрения уже при 16 мм рт. ст., а у других не находят никаких отклонений от нормы и при 27 мм рт. ст. Как и в случае многих других аспектов ПОУГ, причины столь различной чувствительности к уровню ВГД неизвестны.
Симптоматическая глаукома
Симптоматические формы глаукомы имеют характерные признаки, которые врач общей практики должен уметь распознавать, чтобы в дальнейшем направить пациента к специалисту.
Острая закрытоугольная глаукома. Вероятность развития данного заболевания увеличивается с возрастом. В мире частота его встречаемости сильно варьирует, в Европе общая заболеваемость составляет около 0,2%. Следовательно, по крайней мере один раз за свою деятельность врачу общей практики придется столкнуться с этой болезнью.
Острая закрытоугольная глаукома возникает в результате внутренней блокировки угла между радужкой и роговицей корнем радужки из-за функционального сжатия зрачка. Это приводит к нарушению оттока жидкости из задней камеры в переднюю и соответственно повышению ВГД, что автоматически закрывает дренажный угол. В этот момент ВГД резко возрастает до предельно высоких значений (50-80 мм рт. ст.) по сравнению с нормой (15-20 мм рт. ст.).
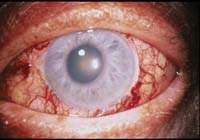 |
| Рисунок 4. Признаки острой закрытоугольной глаукомы: покраснение глаза, помутнение роговицы и неподвижный, овальный, наполовину расширенный зрачок |
В типичном случае пациенту за 60, у него отмечается гиперметропия (дальнозоркость), жалобы на снижение зрения в пораженном глазу и боль вокруг глаза, а также общее плохое самочувствие с тошнотой и рвотой. При обследовании выявляется значительное снижение зрения, покраснение глаза, помутнение роговицы и застывший, наполовину расширенный зрачок (рис. 4).
У некоторых пациентов в анамнезе фиксируется периодическое закрытие угла, когда ВГД колеблется: поднимается и затем снова падает; такие состояния сопровождаются появлением флуоресцентных пятен и радуг вокруг источников света, что вызвано повышенным оттоком жидкости в роговицу под воздействием высокого ВГД. Обычно это происходит вечером, когда зрачок расширен, что еще больше затрудняет отток жидкости. В лежачем положении хрусталик и радужка смещаются назад, что создает условия для облегченного оттока жидкости.
В этой группе пациентов можно спровоцировать развитие приступа закрытоугольной глаукомы путем диагностического расширения зрачка. Однако риск пропустить такие нарушения зрения, как диабетическая ретинопатия, гораздо выше, чем небольшая вероятность вызвать закрытие дренажного угла, поэтому не следует избегать данной диагностической процедуры.
Первоначальные проявления заболевания могут проявляться нетипично. Существует вероятность преобладания общих симптомов, таких как боли в животе, тошнота и рвота.
Спутанность сознания также порой бывает первым признаком острой закрытоугольной глаукомы, что зачастую вводит в заблуждение врача общей практики. Нередко диагностика затягивается, усложняя лечение и увеличивая вероятность необратимой потери зрения.
Что должен сделать врач общей практики? Обычно видно серьезные нарушения в зрении пациента, и в данной ситуации требуется немедленная госпитализация.
При преобладании системных проявлений поставить диагноз трудно, однако следует учесть, что у всех без исключения пациентов обнаруживается красный глаз и ограничение зрения. Пациенты с четкими указаниями в анамнезе на периодическое закрытие угла также нуждаются в незамедлительной консультации специалиста, т. к. истинные пятна не встречаются при мигрени, которая в этом случае является основным дифференциальным диагнозом.
При закрытоугольной глаукоме в первую очередь назначаются препараты, подавляющие продукцию жидкости, такие как ацетазоламид, и капли пилокарпина, чтобы радужка освободила дренажный угол.
Как только ВГД падает и роговица проясняется, производят иридотомию, чтобы через отверстие в радужке некоторая часть жидкости вытекла непосредственно в переднюю камеру. Второй глаз также подвергают иридотомии, т. к. риск закрытия угла в нем очень велик. Как правило, иридотомия производится извне с помощью лазера.
Другие виды глаукомы, сопровождающиеся повышением внутриглазного давления (ВГД). В рассматриваемом разделе будут обсуждены „симптоматические“ глаукомы, так как они связаны с ростом ВГД до критически высоких значений (свыше 40 мм рт. ст.). Такое состояние глаз подвергается ишемии, что вызывает болезненные ощущения, отек роговицы и снижение остроты зрения.
К таким глаукомам относятся следующие.
- Красная глаукома — это состояние, при котором ВГД повышается из-за появления аномальных сосудов в области дренажа, что вторично связано с ишемией сетчатки (см. рисунок 5). Благодаря достижениям в лазерной терапии, диабет сейчас редко становится причиной этой формы глаукомы. Наиболее распространенным триггером красной глаукомы является закупорка центральной венозной системы сетчатки.
- Увеитная глаукома — повышение ВГД, происходящее в результате воспалительного процесса, блокирующего дренажный угол.
- Послеоперационная глаукома — любое хирургическое вмешательство в пределах глаза может провоцировать резкое повышение ВГД. Как правило, такое давление быстро нормализуется.
Врожденная глаукома. Этот вид заболевания встречается не часто, но его наличие необходимо учитывать, так как задержка с диагнозом может негативно сказаться на прогнозе.
Типичный случай выглядит следующим образом: пациент — мальчик (на шесть больных мальчиков приходится четыре девочки) в возрасте до 1 года поступает с избыточным слезотечением и непереносимостью света, при этом родители отмечают, что глаза у ребенка как бы «затуманенные» или «запотевшие».
Эта болезнь может наследоваться по аутосомно-рецессивному типу, поэтому любое упоминание о подобных случаях в семейной истории может повысить вероятность данной диагностики.
При обследовании выявляются увеличенные глаза, что более выражено в случае одностороннего заболевания и помутневшей роговицы, хотя фотофобия затрудняет исследование (рис. 6).
Тем не менее, симптомы заболевания могут быть не всегда очевидными. Двуостороннее увеличение глаз довольно трудно заметить. Избыточная слезоточивость может ошибочно восприниматься как следствие закупорки носослезного канала (в отличие от врожденной глаукомы, при которой наблюдается чередование закупорки и опорожнения канала).
Родительские комментарии типа «с глазами что-то не в порядке» или «он (она) на меня не смотрит» также могут сбить с толку.
К счастью, в большинстве случаев диагноз становится очевидным. Если же этого не происходит, следует обратить внимание на рассказы родителей; такие симптомы, как быстрое увеличение размера глаз, светобоязнь и слезотечение, требуют незамедлительного обращения к специалисту, вне зависимости от результатов обследования.
При светобоязни можно производить обследование при матовом освещении. Если вы не обнаружили отклонений от нормы, но родителей беспокоит состояние зрения их ребенка, направьте их на консультацию к офтальмологу.
Поскольку это заболевание довольно редкое, лечение обычно проводится в специализированных медицинских учреждениях. Как правило, терапия начинается с хирургического вмешательства: с помощью тонкого скальпеля открывается дренажный угол (гониотомия). Если данный метод оказывается неэффективным, может быть выполнена трабекулотомия с последующим выпуском жидкости через субконъюнктивальную дренажную фистулу.
Опыт других людей
Екатерина, 45 лет, домохозяйка: Я всегда считала, что глаукома — это болезнь, которая беспокоит только пожилых людей. Однако в какой-то момент я начала замечать, что плохо вижу в темноте. После посещения врача мне поставили диагноз «комбинированная глаукома». Лечение началось с назначения капель, которые помогают снизить внутриглазное давление. Я узнала, что важно следить за режимом и регулярно посещать врача. Конечно, было страшно, но сейчас я понимаю, что главное — это вовремя выявить проблему и продолжать лечение.
Александр, 60 лет, инженер: Когда мне поставили диагноз «комбинированная глаукома», я был в шоке. У меня не было никаких явных симптомов, и я не ожидал, что со мной может такое произойти. Врач объяснил, что это сочетание открытоугольной и узкоугольной глаукомы, и требуется комплексное лечение. Мой курс включал как капли, так и таблетки. На начальном этапе было сложно привыкнуть к новому режиму, но я старался не пропускать лечение. Врач также рекомендовал специальные упражнения для глаз. Теперь я стараюсь следить за своим состоянием и придерживаться всех рекомендаций.
Мария, 34 года, преподаватель: Узнав о своей диагностике «комбинированная глаукома», я немного растерялась. Оказалось, что эта форма болезни требует более тщательного подхода к лечению. Мой офтальмолог прописал мне несколько видов глазных капель, которые нужно применять несколько раз в день. Я стала более внимательно относиться к своему здоровью, осваивать методы релаксации для снижения стресса, ведь напряжение влияет на зрение. На своем опыте я поняла, как важно следить за регулярными осмотрами у врача, ведь ранняя диагностика — залог успешного лечения.
Вопросы по теме
Как определить, есть ли у меня комбинированная глаукома, и что делать при подозрении на это заболевание?
Комбинированная глаукома — это сложное состояние, которое может проявляться по-разному. Если у вас есть такие симптомы, как ухудшение зрения, болевые ощущения в глазах или изменения в восприятии цветов, вам следует обратиться к офтальмологу для полного обследования. Врач проведет необходимые тесты, такие как измерение внутриглазного давления и осмотр зрительного нерва, чтобы установить диагноз. Если диагноз подтвердится, врач сможет назначить соответствующее лечение.
Какие новые методы лечения комбинированной глаукомы появились в последнее время?
В последние годы в лечении комбинированной глаукомы наблюдается значительный прогресс. Одним из инновационных методов является использование микроскопических имплантатов, которые помогают регулировать давление в глазу. Также исследуются новые медикаменты, которые могут более эффективно снижать давление, улучшая при этом качество жизни пациентов. Важно следить за новостями в офтальмологии и обсуждать с врачом возможности применения современных методов в вашем конкретном случае.
Может ли изменение образа жизни помочь в лечении комбинированной глаукомы?
Да, изменение образа жизни может оказать положительное влияние на течение комбинированной глаукомы. Рекомендуется следить за уровнем физической активности, избегать стрессов и правильно питаться. Регулярные физические нагрузки могут способствовать улучшению циркуляции жидкости в глазу и снижению давления. Кроме того, отказ от курения и ограничение потребления алкоголя также могут способствовать общему улучшению здоровья глаз. Однако изменения в образе жизни должны дополнять, а не заменять основное лечение, назначенное врачом.



