Статья носит информационный характер, не является индивидуальной медицинской рекомендацией. Имеются противопоказания, необходима консультация специалиста.
Диагноз «сомнительный при онкологии» означает, что результаты обследований и анализов не дают однозначного ответа о наличии злокачественной опухоли. В таком случае требуется дополнительное исследование и консультация специалиста, чтобы получить более точную картину заболевания.
В следующих разделах статьи мы рассмотрим, какие методы диагностики используются при подозрении на онкологию, как проводится дифференциальная диагностика между доброкачественными и злокачественными опухолями, а также какие шаги следует предпринять при получении сомнительного диагноза. Вы узнаете, как необходимо действовать, чтобы выявить возможное онкологическое заболевание в ранней стадии и какие возможности современной медицины помогают пациентам с такими диагнозами.
Диагноз сомнительный при онкологии: что означает простыми словами
При обсуждении диагноза сомнительный при онкологии важно понимать его суть. Этот диагноз означает, что результаты исследований и анализов пациента не позволяют сделать окончательное заключение о наличии или отсутствии злокачественной опухоли. В таких случаях врачи предпочитают не делать однозначных выводов, а назначают дополнительные обследования для уточнения ситуации.

Причины возникновения сомнительного диагноза
Сомнительный диагноз при онкологии может возникнуть по разным причинам. Это может быть связано с неоднозначностью результатов биопсии, изменениями на рентгенограммах, неполными данными при медицинском обследовании и другими факторами, которые могут создавать неопределенность в диагностике.
Что делать при сомнительном диагнозе
Если у вас поставили диагноз сомнительный при онкологии, не паникуйте. Важно следовать рекомендациям врача и пройти все назначенные обследования для уточнения диагноза. Не стоит делать поспешных выводов и начинать лечение без окончательного подтверждения наличия опухоли.
Стадии рака: в чем важность их определения
Под термином «онкологическое заболевание» подразумевается множество различных патологий. Однако, существует несколько общих характеристик, которые объединяют более сотни патологий. Эти характеристики включают неправильное строение клеток, вызванное определенной генетической мутацией. Эта мутация приводит к неуправляемому размножению и невосприимчивости к внешним сигналам. В результате, в организме человека образуется злокачественная опухоль. С течением времени, опухоль начинает увеличиваться в размере и распространяться в соседние ткани и органы. Некоторые злокачественные клетки отрываются от опухоли и мигрируют в другие органы, образуя вторичные очаги заболевания, называемые метастазами.
Если не проводить адекватное лечение, заболевание прогрессирует, что делает его более сложноизлечимым. В начальных стадиях рака его можно легко вылечить путем удаления, однако при наличии метастазов возникновение ремиссии практически невозможно.
С целью адекватной определения этапа прогрессирования заболевания была разработана система ранжирования стадий рака. Естественно, для всех заболеваний используются универсальные критерии стадиев, однако у каждого конкретного вида болезни они имеют свои специфические особенности. Корректное определение стадии заболевания является первоочередной задачей для онкологического врача на этапе диагностики.
Необходимость классификации онкологических заболеваний по степеням прогрессирования
Разделение рака на стадии необходимо для решения множества целей: планирование лечения, предсказание прогноза для пациента, так как каждая стадия имеет определенные статистические показатели выживаемости, возникновения ремиссии и возможности рецидива в будущем, контроль хода болезни и эффективность применяемой терапии, обеспечение последовательности в оказании помощи онкологами. Ведь универсальная классификация сглаживает различия между различными языками мира, на которых разговаривают врачи.
TNM является базовой классификацией, используемой повсеместно. Она была разработана в середине 20 века. Последний раз была пересмотрена в 2009 году. Планируется следующая редакция по мере накопления информации о новых достижениях в диагностике и лечении рака.
Аббревиатура используется для классификации злокачественных образований и содержит полезную информацию о их характеристиках:
- Т (tumor) — описывает начальную опухоль;
- N (nodus) — указывает на наличие миграции опухоли в регионарные лимфатические узлы;
- М (metastasis) — говорит о наличии метастазов.
Для определения стадии заболевания к каждой букве присваивается соответствующая цифра или специальное обозначение.
| Описание первичной опухоли | ТХ – первичная опухоль не оценена.Т0 – первичная опухоль не обнаружена.Tis – это ранняя стадия рака, когда обнаруживаются скопления раковых клеток, которые не проникают в соседние ткани.Т1-4 – цифра указывает на размеры опухоли и ее проникновение в соседние ткани. |
| Распространение в регионарные лимфоузлы | NX – оценить состояние регионарных лимфоузлов невозможно.N0 – в регионарных лимфоузлах отсутствуют раковые клетки.N1-3 – цифра указывает на степень поражения регионарных лимфоузлов раковыми клетками. |
| Метастазы | М0 – отсутствуют метастазы.М1 – обнаружены метастазы. |
Часто перед указанием TNM используется дополнительная буква, которая указывает на способ установления диагноза:
- р — диагноз установлен патологоанатомом при изучении опухоли под микроскопом после удаления;
- с — клинический диагноз установлен до проведения биопсии.
Иногда врачи назначают проведение дополнительного исследования, которое называется сентинел биопсией. Это изучение сторожевого лимфатического узла, то есть самого близкого узла, от которого оттекает лимфа от злокачественной опухоли. Это исследование позволяет определить состояние регионарных лимфоузлов и необходимость их удаления и дальнейшего лечения.
Оценка симптомов при подозрении на злокачественный процесс
- боль в определенной области тела;
- изменение формы, размера или текстуры опухоли;
- нарушение функций органов;
- кровотечение;
- отеки на опухолевой области;
- изменение цвета кожи или слизистых оболочек.
Каждый из этих симптомов может указывать на возможное наличие злокачественной опухоли в организме. Они являются особыми и требуют внимания со стороны врача, что позволяет провести дальнейшие исследования и установить диагноз.
Важно отметить, что наличие симптомов, особенно общих и частных одновременно, не всегда является доказательством наличия злокачественного процесса. Однако, их выявление и последующее обследование являются необходимыми этапами для выявления и лечения опухоли на ранней стадии развития, что повышает шансы на полное выздоровление пациента.
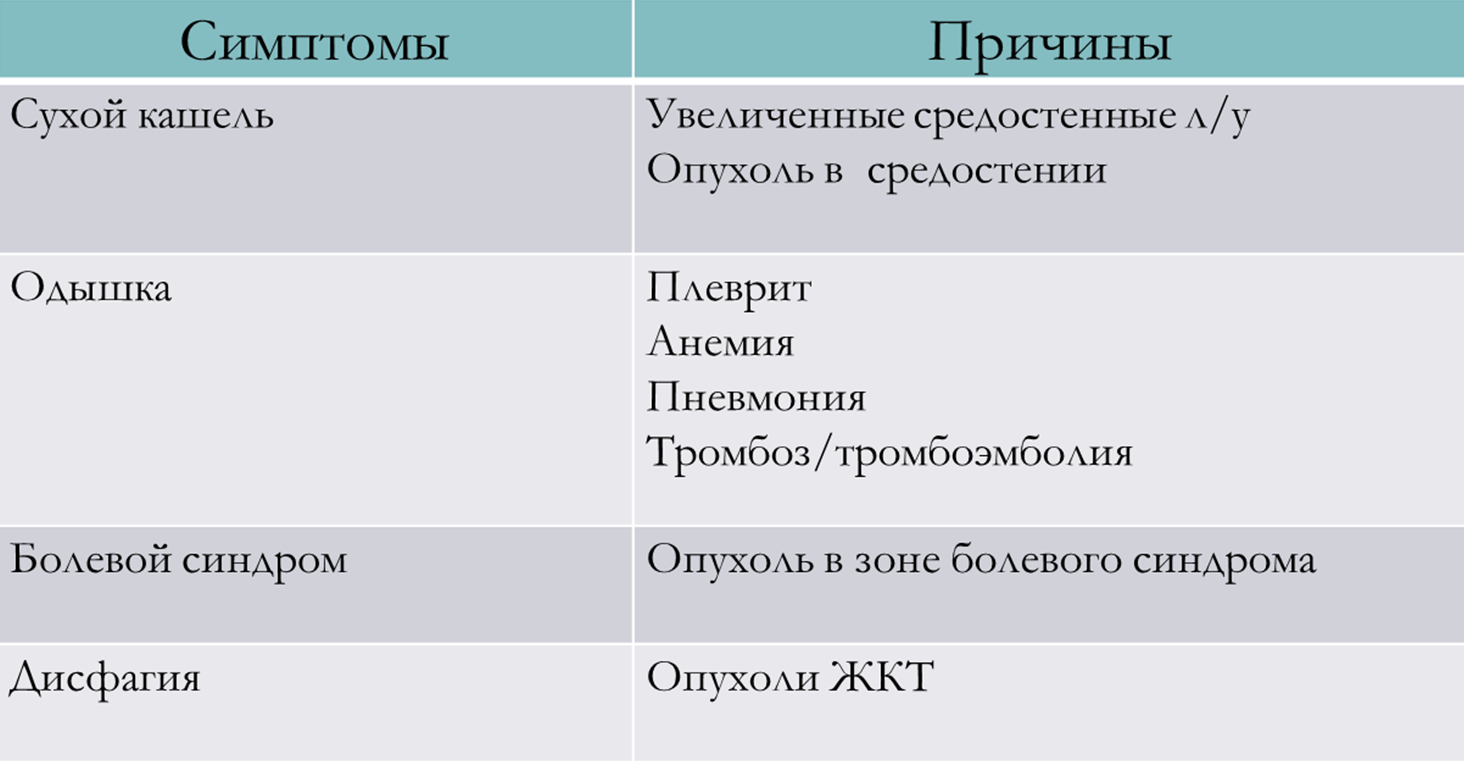
- Длительный искристый кашель (может наблюдаться при опухоли в средостении, опухоли в главных или долевых бронхах, а также при вторичном увеличении лимфатических узлов);
- Длительная одышка при невысокой физической нагрузке или в состоянии покоя (может возникнуть развитие опухолевого плеврита);
- Болевой синдром в области первичного очага опухоли или удаленных метастазов, которые могут сдавливать сосудисто-нервные пучки и вызывать боль у пациента;
- Дисфагия — нарушение прохождения пищи — достаточно частое проявление клинической картины опухолей пищевода или гастроэзофагиальной зоны.
Клинические проявления возможной злокачественной патологии
Диагностические методы, применяемые в онкологии
Первичная диагностика в онкологии, обычно, включает два аспекта:
- Осмотр кожных покровов и слизистых оболочек;
- Пальпация.
В первую очередь необходимо провести визуальную диагностику. Врач осматривает кожу и слизистые оболочки. Это важная часть диагностического процесса, поскольку некоторые опухоли располагаются на тех участках, которые можно оценить визуально, такие как меланома и другие виды рака кожи. Также с помощью пальпации врач может обнаружить увеличенные лимфатические узлы и опухоли мягких тканей.
Для точного выявления заболевания и определения степени развития опухолевого процесса часто требуется проведение различных исследований. Методы диагностики в онкологии делятся на лучевые, эндоскопические и морфологические.
Лучевые методы
Используемые методы лучевой диагностики включают рентгенографию, маммографию, компьютерную томографию (КТ), магнитно-резонансную томографию (МРТ), ультразвуковое исследование (УЗИ) и радиоизотопные методы (позитронно-эмиссионная томография с КТ, остеосцинтиграфия).
Задачи лучевых методов диагностики:
- обнаружение первичного опухолевого образования;
- оценка локального распространения процесса (определение отношения опухоли к окружающим тканям, наличие проникновения в крупные сосуды, наличие инвазии в нервные стволы);
- обнаружение регионарных и отдаленных метастазов;
- биопсия под контролем лучевых методов;
- оценка результатов лечения.
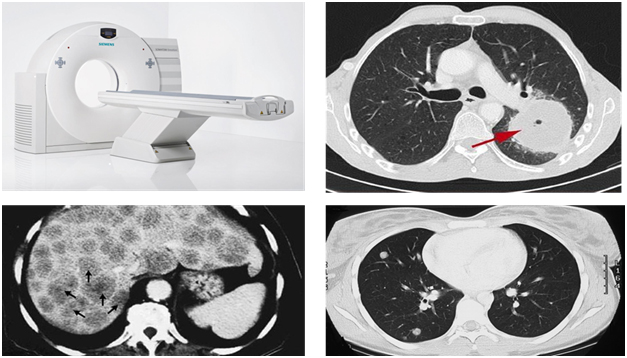
Компьютерная томография
Часто компьютерная томография применяется для визуализации внутренних, то есть паренхиматозных органов. На нижеследующих изображениях компьютерной томографии вы можете увидеть большое первичное образование в легком, а Вторичное метастатическое поражение печени.
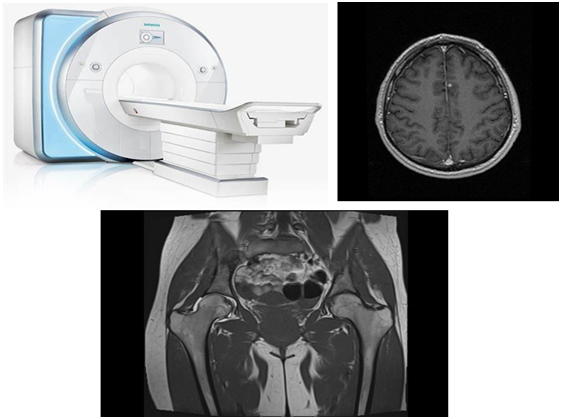
МРТ-обследование
МРТ-обследование чаще всего используется для выявления изменений при исследовании головного мозга и малого таза. Кроме того, медики оценивают не только онкологический процесс, но и все возможные сопутствующие патологии, если они видны на снимках.
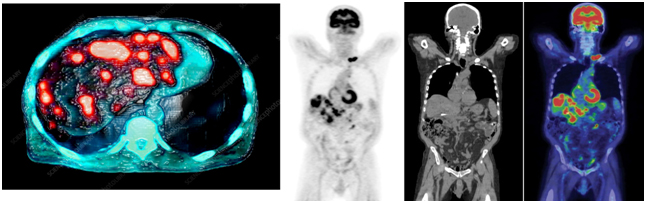
Позитронно-эмиссионная томография (ПЭТ) является процедурой, которая широко используется в медицине. Одной из особенностей этого исследования является использование радиофармпрепаратов, например, радиоактивной глюкозы. Эти препараты вводятся в организм перед проведением томографии.
Кроме определения размера опухоли, ПЭТ-КТ также позволяет оценить метаболическую активность образований. Специалисты могут определить степень накопления радиофармпрепарата в первичных и вторичных опухолях.
Остеосцинтиграфия
Остеосцинтиграфия представляет собой метод радионуклидной лучевой диагностики, при котором осуществляется оценка специфического поражения костей, возникающего вследствие злокачественного процесса.
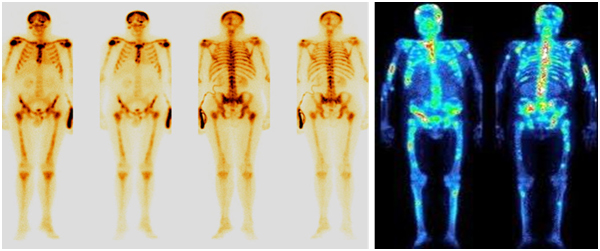
Обязательным моментом является применение радиационных методов исследования для диагностики и оценки степени распространения опухолевого процесса как перед началом лечения, так и во время лечения для контроля за изменением размеров опухоли.
Эндоскопические методы
- выявление предраковых изменений в органах;
- определение степени развития злокачественных опухолей;
- проведение биопсии для морфологических исследований.
- Выбор и обнаружение предраковых изменений слизистой полых органов;
- Дифференциальная диагностика доброкачественных и злокачественных изменений;
- Определение типа роста злокачественной опухоли и уточнение местной распространенности опухолевого процесса;
- Оценка эффективности операционного, радиационного или медикаментозного лечения.
Морфологические методы
В области онкологии диагноз устанавливается только после морфологической верификации обнаруженной опухоли. Для полноценного постановления диагноза, основанного на комплексном подходе, необходимо получить образец пораженной ткани, то есть клетки органа. Для получения образца ткани для дальнейшего исследования используется биопсия.
Биопсия может быть выполнена в нескольких вариантах:
— Тонкоигольная биопсия;
— Трепан-биопсия;
— Эксцизионная биопсия;
— Инцизионная биопсия.
Цель любого из этих вариантов биопсии заключается в получении материала для последующего морфологического исследования.
С использованием методов морфологии определяется тканевое происхождение опухоли с целью понимания ее гистотипа (гистологической структуры опухолевой ткани и ее особых характеристик). При диагностике учитываются особенности нетипичных клеток, также проводится оценка полей некроза, кровоизлияний, определяются форма и количество питающих сосудов.
Необходимость проведения морфологической дифференцировки и диагностики является основополагающей в онкологии. Морфологические методы можно разделить на гистологические и иммуногистохимические исследования.
В некоторых случаях для выбора эффективного лечения или более детального изучения диагноза требуется выполнить комплекс иммуногистохимических исследований, так как наличие определенных маркеров позволяет определить наиболее эффективную тактику медикаментозного лечения для пациента.
Наиболее часто определяемые иммуногистохимические маркеры:
- ER (эстрогеновый рецептор);
- PR (прогестероновый рецептор);
- Her2/neu (рецептор фактора роста эпидермальных клеток);
- Ki67 (индекс активности пролиферации, может измеряться для всех типов опухолей. Определяет скорость роста опухоли, риск метастазирования и эффективность терапии);
- PD-L1 (трансмембранный белок, связывающийся с рецептором PD-1 на цитотоксических лимфоцитах и блокирующий их цитотоксическую активность).
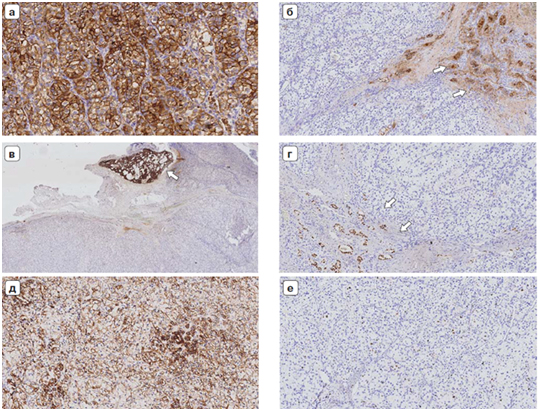
Молекулярно-генетические исследования проводятся для различных целей:
- Для пациентов с уже диагностированными онкологическими заболеваниями, чтобы определить наиболее подходящую и эффективную терапию. Например, такими исследованиями можно определить микросателлитную нестабильность — генетическую изменчивость опухолей, чтобы назначить иммуноонкологические препараты.
- Для здоровых людей с наследственной предрасположенностью к онкологии. Например, рекомендуется определить мутацию BRCA у молодых здоровых женщин, чьи кровные родственники (мать, бабушка) имели злокачественные опухоли молочной железы.
У одного и того же типа рака опухоль может иметь различную биологию. Таргетная терапия подбирается индивидуально в зависимости от молекулярно-генетических характеристик обнаруженной опухоли. Молекулярно-генетические маркеры необходимы для подробного дифференцирования опухоли и определения места применения таргетной терапии. Ниже перечислены лишь некоторые мутации, которые могут возникать при различных злокачественных образованиях: BRAF, EGFR, с-kit, KRAS, NRAS, ALK, ROS1, MET. Для каждой из них применяются определенные таргетные препараты, которые эффективно лечат конкретное заболевание.
Адекватная диагностика – важный аспект успешного курса лечения онкологической патологии. Если врач объясняет пациенту необходимость проведения дополнительных исследований или требуется выполнить определенные иммуногистохимические тесты, важно следовать рекомендациям специалиста. В результате онколог-врач сможет более глубоко исследовать проблему и назначить оптимальный план лечения.
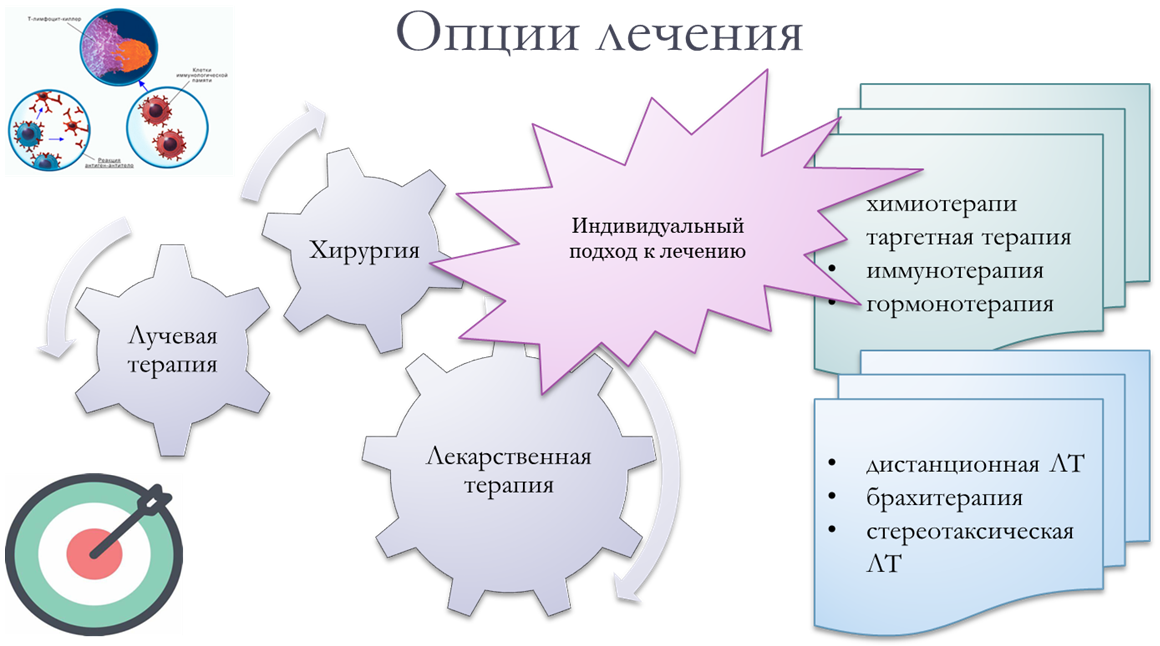
Весь поиск, оценка распространения процесса, определение по гистологическим и иммуногистохимическим параметрам необходимы для индивидуального подхода к лечению.
В настоящее время доступно множество вариантов лечения — хирургическое вмешательство, лучевая терапия, различные виды медикаментозного лечения. Чем больше знаний врача о характере и особенностях вашего заболевания, тем больше возможностей и шансов на борьбу с раком.
О чем говорит отклонение от нормы
В отрасли онкологии, путем анализа уровня специфических белков, определяют стадию заболевания, а по их разнообразию — предполагаемое место появления новообразования.
Также, наличие связанного рака может указывать на наличие опухолей, инфекций, воспалительных процессов и других доброкачественных заболеваний.
Обратите внимание: небольшое количество онкомаркеров может присутствовать в крови здоровых людей.
Ниже приведены данные о нормальном содержании таких веществ в организме и возможных проблемах, возникающих при отклонении от этих показателей.
| Онкомаркер | Максимальное нормативное значение | Вероятное расположение опухоли | Возможные прочие заболевания |
| ПСА | 4 нг/мл | Предстательная железа | Инфекционный простатит; аденома. |
| СА-125 | 30 МЕ/мл | Женская репродуктивная система; поджелудочная железа; ЖКТ; дыхательные органы (редко). |
Отдельно следует отметить маркер АФП. В гинекологии его использование связано с оценкой состояния беременности. В онкологии он указывает на возможное развитие рака печени, яичников, молочной железы, бронхов и легких, ЖКТ.
Для беременных уровни АФП в норме следующие:
- до 12 недели — менее 15 Ед/мл;
- 13-15 недель — от 15 до 60 Ед/мл;
- 15-19 недель — от 15 до 95 Ед/мл;
- 20-24 недели — от 27 до 125 Ед/мл;
- 25-27 — от 52 до 140 Единиц/миллилитр;
- 28-30 — от 67 до 150 Единиц/миллилитр;
- 31-32 — от 100 до 250 Единиц/миллилитр.
Обратите внимание: превышение указанных значений может указывать на наличие патологий в развитии плода.
Кроме того, повышенный уровень АФП является признаком гепатита или цирроза.
На основе представленных данных в таблице можно сделать вывод, что отклонения в показателях конкретного онкомаркера указывают на вероятность возникновения различных заболеваний. Однако, основываясь только на содержании специфических белков в крови, невозможно поставить диагноз. Для подтверждения или опровержения наличия раковой опухоли в организме требуются дополнительные диагностические процедуры.
Надежность маркеров в онкологии
Анализ содержания данных веществ является важным инструментом для оценки эффективности прописанного терапевтического курса при онкологическом заболевании. Однако, ни один из этих маркеров не используется в качестве самостоятельного метода первичной диагностики из-за их недостаточной специфичности.
Достоверность данных о специфических белках может быть объяснена с использованием наиболее распространенных примеров. Один из таких примеров — это тест ПСА. Этот биомаркер используется для своевременного выявления рака предстательной железы у мужчин. Уровень данного показателя действительно повышается при злокачественных опухолях предстательной железы.
Однако, он может увеличиваться при наличии доброкачественных новообразований в предстательной железе. По медицинской практике, у большинства мужчин с повышенным уровнем ПСА не обнаруживается рак предстательной железы.
Обратите внимание: существуют случаи, когда недобросовестные врачи в подозрительных клиниках назначают ненужные терапевтические процедуры. Они не только требуют значительных финансовых затрат, но также могут вызвать серьезные осложнения!
Другим определением, которое можно использовать в медицинском контексте, является CA-125. Уровень данного определителя увеличивается в крови женщин с раком яичников, однако он также может повышаться при других патологиях, не связанных с онкологией.
Врачам известны случаи, когда уровень данного определителя в крови не показывал отклонений у пациенток с поздними стадиями развития злокачественных новообразований в яичниках, несмотря на наличие 28 специфических белковых соединений, характерных для данного заболевания.
Не рекомендуется проводить исследование CA-125 на ранних стадиях болезни, если отсутствует характерная симптоматика. Для оценки хода заболевания данный определитель рассматривается вместе с другими белками и результатами ультразвукового исследования.
В рамках комплексного обследования женщины с плохой наследственностью или генными мутациями должны сдавать онкомаркеры каждые полгода.
Существует открытый вопрос о том, насколько можно доверять данным, полученным с использованием онкомаркеров. При анализе результатов необходимо учитывать ряд факторов, которые могут исказить данные:
- Воспалительные заболевания в острой или хронической форме могут повлиять на уровень содержания белков;
- Уровень СА-125 может повышаться во время менструации;
- У курильщиков наблюдается двукратное увеличение показателя РЭА;
- Нормальные результаты анализов не гарантируют отсутствие новообразования.
