Статья носит информационный характер, не является индивидуальной медицинской рекомендацией. Имеются противопоказания, необходима консультация специалиста.
Клетки цилиндрического эпителия с дистрофией в желудке — это изменение, которое может указывать на нарушения в работе пищеварительной системы. Дистрофия клеток эпителия может привести к болевым ощущениям, нарушению пищеварения и другим негативным последствиям.
Далее в статье мы рассмотрим основные причины дистрофии клеток цилиндрического эпителия в желудке, а также какие меры предосторожности можно принять для предотвращения данного заболевания. Мы также расскажем о методах диагностики и лечения дистрофии, а также дадим рекомендации по правильному питанию и образу жизни для поддержания здоровья желудочно-кишечного тракта. Не упустите возможность узнать больше об этом важном заболевании и способах его профилактики!
Клетки цилиндрического эпителия с дистрофией в желудке: понятие и особенности
Цилиндрическое эпителий — это один из типов тканей, которые образуют внутреннюю поверхность желудка. Данный тип эпителия характеризуется тем, что его клетки имеют форму цилиндра и строятся в виде многослойного слоя.

Что такое дистрофия в желудке?
Дистрофия в желудке — это патологическое состояние, при котором клетки цилиндрического эпителия подвергаются дегенерации и структурным изменениям. Это может привести к нарушению функций желудка и возникновению различных заболеваний.
Особенности клеток цилиндрического эпителия с дистрофией
Клетки цилиндрического эпителия, пораженные дистрофией, могут иметь измененную форму, размер и функциональные свойства. Они могут потерять способность к правильному выделению секрета желудка или поглотительной функции. Такие изменения, если не обнаружены и не лечатся своевременно, могут привести к серьезным последствиям для здоровья пациента.
Как облегчить состояние при кишечной метаплазии
Патогенез данного заболевания обусловлен постепенной атрофией слизистого эпителия желудка, с последующей трансформацией его в эпителий толстого или тонкого кишечника. Измененная слизистая оболочка начинает выполнять функции того органа, к которому она по факту принадлежит. Это приводит к потере желудком своих функций как органа пищеварения, с соответствующими негативными последствиями.
Метаплазия является редкими патологиями пищеварительной системы и не является самостоятельным заболеванием. Она возникает только при длительном хроническом повреждении слизистой оболочки органа на фоне воспалительного процесса. Это состояние представляет угрозу для здоровья и жизни человека. Тем не менее, своевременная диагностика и комплексное лечение позволяют полностью выздороветь.
Разновидности метаплазии
В гастроэнтерологии выделяют следующие виды кишечной метаплазии или атрофии:
- Толстокишечная (незрелая или неполная). Этот вид метаплазии самый опасный, так как он может привести к злокачественному перерождению.
- Тонкокишечная (зрелая или полная). В отличие от предыдущего варианта, этот вид метаплазии не связан с риском онкологии.
Помимо указанных двух типов, Возможно развитие смешанной формы кишечной метаплазии слизистой, когда в желудке обнаруживаются клетки эпителия как толстого, так и тонкого кишечника.
В зависимости от степени распространения выделяют следующие формы метаплазии:
- Выраженная форма. Более 20% поверхности стенок желудка содержит клетки эпителия кишечника.
- Умеренная форма. Площадь поражения желудка составляет не более 20%.
- Слабо выраженная форма. В данном случае, клетки кишечного эпителия покрывают не более 5% площади желудка.
Также существует классификация этого заболевания по характеру распространения. Выделяют следующие виды метаплазии:
- Диффузная. Патологические изменения в желудке локализуются в антральном и пилорическом отделах. При развитии болезни, клетки кишечного эпителия могут распространяться и на фундальный отдел органа.
- Очаговая. Эта форма заболевания характеризуется локальными изменениями клеточного состава слизистой оболочки желудка в антральном и пилорическом отделах. Процесс развивается из-за нарушения естественного обновления клеток и при длительном вялотекущем воспалительном процессе.
Абсолютная тонкокишечная метаплазия
Данное состояние характеризуется появлением клеток эпителия тонкого кишечника на всей поверхности желудка. Одним из характерных признаков абсолютной тонкокишечной метаплазии является появление клеток Панета. По структуре и функциональным особенностям, желудок полностью схож с тонким кишечником. Чаще всего данная форма метаплазии сопровождается хроническим гастритом.
Частичная толстокишечная метаплазия
У данного заболевания не характерно появление клеток Панета, однако наблюдается возникновение эпителиальных клеток, которые покрывают внутреннюю поверхность толстого кишечника. При метаплазии толстого кишечника возможны нарушения процесса дифференцирования и созревания клеток, что указывает на высокий риск формирования злокачественной опухоли.
Клетки цилиндрического эпителия с дистрофией в желудке что это
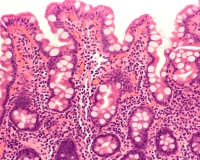
В процессе цитологического изучения материала, полученного из желудка при помощи гастробиопсии, в препаратах ясно видны клеточные структуры слизистой оболочки желудка: покровно-ямочный эпителий, главные и обкладочные клетки желез.
Соотношение клеточных структур слизистой оболочки желудка, их уровень дифференцировки, появление признаков дегенерации и атипии, а также наличие лейкоцитов, ретикулярных и гистиоидных элементов позволяют определить типы гастроцитограмм, которые характерны для различных заболеваний желудка.
Для пациентов, страдающих хроническим гастритом, характерна наличие клеток покровно-ямочного эпителия, которые образуют небольшие группы и скопления. Форма клеток может быть высоко- или низкоцилиндрической, а ядро может быть расположено в основании или в центре. Цитоплазма клеток имеет широкую и слабо-базофильную структуру. Ядра клеток имеют некоторую вариабельность их формы, начиная от несозрелых больших ядер с нежным сетчатым рисунком хроматина, заканчивая зрелыми, небольшими и интенсивно окрашенными ядрами.
Имеются различные количества главных и обкладочных клеток желез, которые располагаются неупорядоченно в виде небольших круглых групп или прямых рядов, где наблюдается правильное чередование главных и обкладочных клеток. В главных клетках явно видны крупные гранулы, окрашенные в сине-фиолетовый цвет, заполняющие всю цитоплазму. Обкладочные клетки отличаются широкой светлой цитоплазмой, окрашенной в нежно-розовый цвет. В препаратах встречаются лимфоидные элементы и нейтрофильные лейкоциты с множественными ядрами.
В анализе мазков при образованиях в желудке наблюдается большое количество слоев и крупных скоплений эпителия с ямочками, а также обнаруживаются структуры, подобные железистым. В сравнении с анализами при гастрите можно отметить преобладание молодых, незрелых клеток с увеличенными ядрами и нежным рисунком хроматина в них.
При развитии язвенной болезни желудка в анализах обнаруживается преобладание нейтрофилов с сегментированными ядрами, а также значительное количество лимфоцитов, плазматических клеток, эозинофилов и клеток гистиоцитарного типа, а также скопления полиморфных эпителиальных клеток. В эпителии обычно наблюдаются признаки дегенерации в виде образования вакуолей в цитоплазме и ядрах, кариолизиса, кариорексиса и плазмолиза.
При анализе клеток материала при неопухолевых и опухолеподобных поражениях желудка, возникают определенные трудности в постановке диагноза. Это связано с тем, что изменения в клетках имеют схожий характер и часто можно оценить только степень клеточной пролиферации, аномалий и перестройки эпителия в соответствии с кишечным типом.
Среди злокачественных новообразований в желудке наиболее распространены три типа аденокарциномы: высоко- и низкодифференцированные аденокарциномы, а также аденокарцинома с обильным секрецией слизи. Реже встречаются перстневидноклеточный рак, недифференцированный рак, а также другие неэпителиальные опухоли.
У пациентов с раком желудка наблюдаются цитограммы, которые характеризуются наличием клеток со злокачественными морфологическими признаками. Клетки располагаются в комплексах, которые могут быть железисто-подобными или иметь папиллярную структуру, разрозненно. В комплексах и структурах наблюдается хаотическое скопление ядер. Клетки имеют большие размеры. Ядра занимают практически всю клетку и имеют преимущественно неправильную форму. Они содержат гиперхромное, грубое и неравномерно распределенное хроматиновое вещество, а также гипертрофированные множественные нуклеолы.
Установить гистологическую форму опухоли не всегда возможно, чаще всего это происходит в случаях аденокарциномы, где обычно обнаруживаются структуры, похожие на железистые. Коллоидный рак характеризуется наличием большого количества слизистых масс и клеток опухоли в форме перстневидных колец. При малодифференцированном раке наблюдаются сильно анаплазированные клетки, с большим количеством фигур деления, которые обычно располагаются в разрозненном порядке.
Общие сведения
Интестинальная метаплазия, которая проявляется в кишечной зоне желудка, является одной из наиболее актуальных проблем в сфере гастроэнтерологии и онкологии. Это состояние может прогрессировать в дисплазию, которая является предраковым состоянием слизистой оболочки желудка. Истинная частота данной проблемы неизвестна, поскольку она не имеет специфических признаков и редко обнаруживается вовремя. Морфологическое понятие кишечной метаплазии отражает сущность патологических изменений в желудочной зоне, поэтому пациентам обычно ставят диагноз хронического гастрита согласно общепринятой классификации.
Предраковые заболевания желудка

Обязательный предрак — это заболевания, которые всегда или в большинстве случаев, если их не лечить, приводят к развитию рака. К таким заболеваниям относятся язвы желудка, антральный гастрит с повышенной жесткостью, полипы и полипоз желудка.
Факультативный предрак — это хронические заболевания желудка, при которых рак развивается относительно редко, но чаще, чем у здоровых людей. Это атрофический гастрит, болезнь после операции желудка, пернициозная анемия, Менетрие и другие.
Национальный раковый конгресс в Японии объединяет некоторые заболевания, которые могут привести к раку желудка, как фоновые, включая обязательный и факультативный предрак в одну группу.
- Согласно данным Национального ракового конгресса, рак желудка может формироваться на фоне хронического атрофического гастрита в 0-13% случаев, пернициозной анемии — в 0,5-12,3%, хронической язвы желудка — в 1-2%, гиперпластического полипа — в 1-2%, плоской аденомы — в 6-21%, папилловирусной аденомы — в 20-75%, болезни Менетрие — в 5-10%, а также после резекции желудка — в 0,4-7,8% случаев.
- Подавляющее большинство специалистов считает, что при развитии опухолевого процесса эпителиальные клетки слизистой оболочки желудка претерпевают последовательные изменения: нормальный эпителий -> пролиферирующий -> атипические клетки -> злокачественная опухоль.
- С морфологической точки зрения, участки пролиферации атипического эпителия, размещенные мультисентрически, называются дисплазией.
Дисплазия является нарушением структуры ткани, которое характеризуется патологическим ростом и изменением эпителия. В слизистой оболочке желудка можно выделить три степени дисплазии (легкая, умеренная и тяжелая).
У дисплазии I и II степени изменения слабо выражены и могут быть обратимыми. Однако изменения, связанные с дисплазией III степени, являются постоянными и могут рассматриваться как рак in situ. У 40-45% пациентов старше 60 лет происходит изменение эпителия слизистой оболочки желудка, которое принимает форму кишечного типа — кишечная метаплазия (тонкокишечная, толстокишечная). Толстокишечная метаплазия рассматривается как предраковое состояние.
Хронический гастрит является наиболее распространенным заболеванием среди патологии органов пищеварительной системы, его доля составляет 35% от всех заболеваний этой системы и 85% от заболеваний желудка.Хронический гастрит является полиэтиологическим заболеванием. Существует множество факторов, которые вызывают его, однако в соответствии с этиопатогенезом их можно объединить в три основные группы:
•I группа — инфекционные (экзогенные) гастриты, вызванные желудочным хеликобактером (гастрит В — бактериальный);•II группа — аутоиммунные гастриты, обусловленные образованием антител к обкладочным клеткам желез желудка (гастрит А — аутоиммунный) — атрофический гастрит;•III группа — гастриты, связанные с частичными термическими раздражениями и медикаментозными воздействиями, проявляющиеся гастродуоденальным рефлюксом (гастрит С — реактивный или химический).В 0-13% случаев на фоне хронического атрофического гастрита возникает рак желудка.
Клиника.
Клиническая картина хронического гастрита не имеет характерных типичных признаков, которые позволили бы определить его формы.
Основные жалобы: нарушение аппетита, неприятные ощущения в области эпигастральной, связанные с приемом пищи, отрыжка, изжога, тошнота, иногда рвота.
Сочетания симптомов желудочной и кишечной диспепсии могут быть разнообразными (ощущение полноты желудка после еды, вздутие живота, руминация, боли, сменяющиеся запорами и поносами).
Диагностика.
Рентгенологические методы исследования в диагностике хронического гастрита имеют относительную значимость. Они более эффективны для обнаружения язвенных, полипозных и опухолевых поражений желудка. Исключением является ригидный антральный гастрит.
Определяющую роль в выявлении различных форм хронического гастрита играют гастрофиброскопия и гастробиопсия. Диагноз (цитологический и гистологический): кишечная метаплазия, дисплазия разной степени выраженности, инфекция, вызванная Helicobacter pylori (HP).
В лечении хронического гастрита неинфекционной этиологии проводятся следующие терапевтические мероприятия: устранение основных причин, способствующих развитию или поддержанию заболевания, применение диетотерапии, использование седативных средств в период обострений, применение средств, улучшающих микроциркуляцию и питание слизистой оболочки, проведение витаминотерапии и санаторно-курортное лечение.
Особую важность приобретает инфекционный гастрит, вызванный бактериями Helicobacter pylori. Согласно научным исследованиям, половина населения планеты, а именно 30-50%, являются носителями данной инфекции (человек с заболеванием или переносчик бактерий). HP-бактерии обычно размножаются под слоем слизи, находящейся над слизистой оболочкой привратника. Они присоединяются к верхушкам клеток эпителия, выделяют определенные ферменты, включая цитотоксины и уреазу, и вызывают развитие отека, гиперемии, нарушения питания и дегенерации клеток слизистой оболочки. Воспалительные и атрофические процессы тесно связаны друг с другом и имеют инфекционно-иммунологическую природу.
В последние 10 лет многочисленные исследования изучают проблемы, связанные с хеликобактериозом и раком желудка. Сейчас научно подтверждено, что Helicobacter pylori производит множество патогенных ферментов и токсинов, некоторые из которых могут играть роль в возникновении рака.
• Установлена связь между наличием инфекции Helicobacter pylori (HP) и разновидностью неполной кишечной метаплазии, которая считается предраковым состоянием.• Определено, что HP с помощью экстрацеллюлярной уреазы расщепляет мочевину, образуя аммиак, активизирует процессы перекисного окисления липидов и повышает концентрацию свободных радикалов – продуктов кислорода, что способствует развитию рака.• В in vitro экспериментах доказана способность HP стимулировать рост опухолевых клеток.Рак желудка часто сопровождается инфицированием слизистой оболочки HP. Инфекция HP распространена шире, чем при язвенной болезни, и охватывает все отделы желудка, включая саму опухоль.
Хеликобактерный гастрит (гастрит В) требует специализированного лечения. Для эффективного уничтожения данных бактерий необходимо обязательное применение трех препаратов с антибактериальной активностью: амоксициллин или ампициллин, метронидазол (производный нитронидазола) и фуразолидон (производный нитрофурина). Базисный препарат — де-нол (соль лимонной кислоты, содержащая висмут).
Диагностирование гиперплазии

Гиперплазия представляет собой процесс, при котором происходит неправильный рост клеток в организме. Для выявления данного состояния необходимо провести внутреннее исследование проблемного органа. Врачи используют специальное медицинское оборудование, чтобы решить эту задачу.
Чтобы подтвердить диагноз гиперплазии, пациенту рекомендуется пройти следующие исследования:
- Рентгенография. Данный метод позволяет увидеть количество полипов, которые образуются в желудке из-за данного заболевания. Врач может обнаружить опухоль, если она уже сформировалась.
- УЗИ органов желудочно-кишечного тракта. Это исследование дает аналогичный результат рентгенографии.
- Метод фиброгастродуоденоскопии представляет собой одну из процедур, которая может быть неприятной для пациента, но она обеспечивает точные результаты, чтобы врач мог полностью оценить характер заболевания. Путем введения специального аппарата внутрь органа, врач может подробно изучить полипы и другие аномалии.
- Биопсия — важный метод, который позволяет определить злокачественность новообразования в желудке, вызванного гиперплазией.
Получение точного диагноза полипов в желудке может быть затруднено при использовании биопсии и эндоскопии. При этом заболевании часто возникают псевдонаросты, которые трудно отличить от истинных образований.
Рацион при гиперплазии органа пищеварительной системы

Для достижения положительных результатов в лечении, необходимо прежде всего пересмотреть рацион питания пациента. В случае наличия патологии желудка, рекомендуется употреблять следующие продукты:
Врач обязательно должен ознакомить пациента с особенностями питания во время лечения и периода восстановления. Эта диета также может быть рекомендована в качестве профилактической меры для предотвращения повторного возникновения заболевания.
Клетки эпителия в желудочном содержимом
Клетки эпителия слизистой оболочки желудка обнаруживаются как отдельно, так и вместе с лейкоцитами в слизистых скоплениях. В кислой среде эпителиоциты желудка имеют форму овальных (круглых) ядер и располагаются рядом друг с другом. Это отличает их от ядер эпителиоцитов полости рта и пищевода, которые, из-за большого размера клеток, находятся значительно удалены друг от друга. В желудочном содержимом с низкой кислотностью эпителиоциты слизистой оболочки желудка сохраняют свою цилиндрическую форму.
В случае гипертрофического гастрита, клетки эпителия желудка обычно образуют группы, скопления, пласты и слепки из желудочных желез. Иногда они могут обнаруживаться в большом количестве в кровянисто-окрашенных плотных образованиях. В некоторых случаях эти клетки подвергаются слизистой и жировой дистрофии, а также метаплазии, в результате чего они становятся округлыми и уплощенными. При гипертрофическом гастрите обычно наблюдается большое количество эпителиоцитов слизистой оболочки желудка, особенно в области пилорической части, где происходит воспалительный процесс.
При полипах желудка обнаруживаются пласты однотипного цилиндрического эпителия, которые свидетельствуют о пролиферации. В этих пластах можно наблюдать двух- или трехъядерные клетки с увеличенными ядрами, а некоторые из них содержат ядрышки.
При наличии рака желудка может наблюдаться обнаружение атипичных эпителиоцитов в компактных кластерах и слизи, иногда они располагаются в виде групп и имеют железистый вид, также не редко встречается вакуольная или жировая дистрофия.
При заболевании лимфогранулематозом можно наблюдать наличие клеток Березовского—Штернберга, при туберкулезе — гигантских клеток Пирогова—Лангханса, при актиномикозе — друз актиномицет.
Компоненты пищи в содержимом желудка
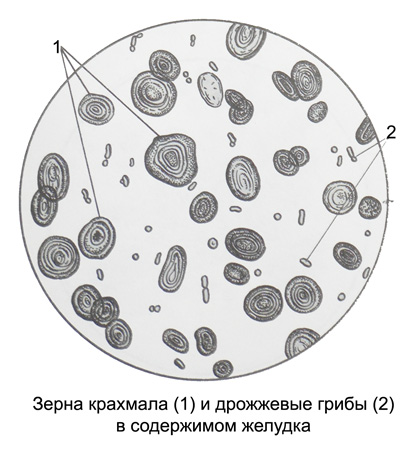
При микроскопическом анализе желудочного содержимого возможно обнаружение зерен крахмала, дрожжевых грибов, липидов и мышечных волокон.
Зерна крахмала являются основными компонентами хлеба, картофеля, бобовых и некоторых других продуктов.
Разложение углеводов происходит под воздействием фермента амилазы (птиалина), который активируется в щелочной среде. В результате этого крахмал сначала разлагается на амидулин или амилодекстрин — растворимую форму крахмала, которая при наличии йода окрашивается в фиолетовый цвет. Следующим этапом разложения является образование эритродекстринов, которые окрашиваются в красноватый цвет при воздействии раствора Люголя. В конечном итоге появляются ахродекстрины и мальтоза, которые не реагируют на йод.
Разложение крахмала прекращается в желудке, то есть в кислой среде. Чем выше кислотность, тем раньше амилаза теряет свою активность. При наличии ахлоргидрии разложение крахмала продолжается до образования ахродекстринов и мальтозы.
Таковым образом, при увеличенной кислотности содержимого желудка выявляются фиолетово-измененные гранулы крахмала (амидулин), при нормальной кислотности – гранулы в основном красноватого цвета (эритродекстрины), при отсутствии кислотности в результате образования ахродекстринов и мальтозы окрашивание отсутствует, большая часть крахмала расщепляется полностью.
Дрожжевые грибы — овальные, сильно отражающие свет образования сферической формы, образующие типичные почковидные структуры (восьмерки). При добавлении раствора Люголя они получают желтый цвет. Дрожжевые грибы вместе с гранулами крахмала выявляются в содержимом желудка после хлебного пробного завтрака или обнаруживаются при задержке пищи в желудке.
В желудочном содержимом пациента с признаками застоя образуются различного размера капли нейтрального жира, которые окрашиваются суданом III в оранжево-красный оттенок.
В содержимом желудка пациента с низкой кислотностью обнаруживаются мускульные волокна, имеющие форму цилиндрических желтовато-зеленых образований с характерным поперечным рисунком. Присутствие этих образований указывает на наличие застойных явлений в желудке.
При микроскопическом исследовании желудочного содержимого иногда обнаруживаются микроорганизмы, включая сарцины и палочки молочнокислого брожения.
Сарцины — это кокки, которые разделяются в трех перпендикулярных плоскостях и по своему внешнему виду напоминают перевязанные тюки.
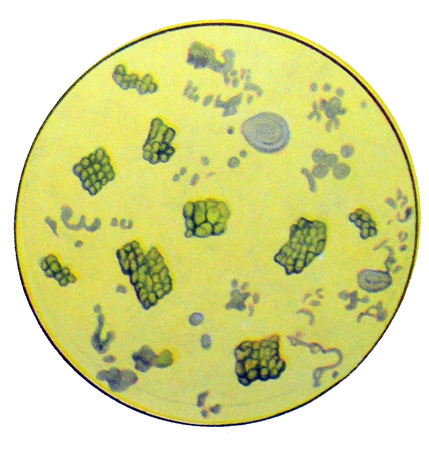
При нарушении соударения пищевых масс и наличии свободной соляной кислоты в содержимом желудка возможно обнаружение палочек молочнокислого брожения. Палочки молочнокислого брожения (Боаса—Оплера) — это длинные, грубые, слегка изогнутые палочки, которые часто находятся под углом. Они обнаруживаются при замедленной эвакуации пищи из желудка в случае отсутствия свободной соляной кислоты.
Что такое Исследование содержимого двенадцатиперстной кишки?
Гипокинетический тип дискинезии желчного пузыря характеризуется увеличением времени выделения порции В до более 60 мин и уменьшением объемной скорости выделения желчи и увеличением объема порции В до более 200 мл. Гиперкинетический тип дискинезии желчного пузыря характеризуется сокращением времени выделения порции В (менее 20 мин), увеличением объемной скорости выделения желчи (более 5 мл/мин); объем порции В практически не изменен.
Желча является секретом печеночных клеток, имеет жидкую форму и относительную плотность в диапазоне 1,007-1,015. Она обладает щелочной реакцией (рН 7,3-8,0) и имеет золотисто-желтую окраску в порциях А и С, а в порции В — темно-оливковую или коричневую. При прохождении по желчным протокам и во время нахождения в желчном пузыре, желчь претерпевает некоторые изменения. К печеночной желчи добавляется секрет эпителия желчных путей и желчного пузыря, содержащий много муцина. Это придает желчи густую и вязкую консистенцию.
Стало понятно, как возникает предраковое состояние пищевода — синдром Барретта

Иллюстрация 1. Схематическое представление области перехода между пищеводом (Oesophagus) и желудком (Stomach) с изображением эпителиальных клеток различных типов. Переходный эпителий (Transitional epithelium) состоит из базальных (Basal layer) и люминальных (Luminal layer) клеток, которые выражают трое белков-маркеров (p63, KRT5 и KRT7) на разном уровне. Рефлюкс желчными кислотами или нарушение экспрессии определенных генов могут привести к превращению пограничной области эпителия в аномальный эпителий, подобный эпителию кишечника, с наличием бокаловидных клеток (Goblet cell), и формированию структуры, известной как пищевод Барретта (Barrett’s oesophagus). Отрывок из популярной аннотации к обсуждаемой статье
Научным исследователям удалось раскрыть механизм формирования преканцерозного состояния в зоне соединения пищевода и желудка, известного как синдром Барретта. Исследователям удалось детально описать эпителий в этой граничной области и эксперименты на лабораторных мышах показали, что базальные клетки с определенным набором маркеров имеют потенциал стать предшественниками ткани, аналогичной ткани кишечника, которая заменяет нормальный эпителий в данной области. Клетки с аналогичными свойствами также были найдены на границе пищевода и желудка у человека, что делает данное исследование потенциально полезным для улучшения методов ранней диагностики и лечения онкологических заболеваний.
Отлично известно, что чем раньше обнаружить и начать лечение онкологического заболевания, тем проще будет само лечение и тем больше вероятность выздоровления. Для некоторых видов рака имеются предраковые состояния — изменения в тканях, которые сами по себе не являются злокачественными, но увеличивают риск развития рака в этих тканях. Пока такие состояния известны для ограниченного числа раковых заболеваний. Поэтому необходимо, с одной стороны, стремиться расширять список соответствий между злокачественными опухолями и предраковыми состояниями, а с другой стороны, разбираться в механизмах возникновения этих состояний, чтобы повысить эффективность профилактики рака.
Одно из предраковых состояний называется метаплазией. В этом состоянии клетки одного типа замещаются клетками другого типа, что часто происходит на границах разных типов эпителия. В таких случаях метаплазия может привести к развитию злокачественных опухолей эпителиальных клеток, известных как карциномы.
Эпителий — это ткань, которая покрывает поверхность тела, внутренние полости и слизистые оболочки органов. В медицине России выделяют два основных вида эпителия: многослойный плоский эпителий (кожа, слизистые оболочки, пищевод) и однослойный цилиндрический эпителий (желудок, кишечник). Также существует переходный эпителий, который выстилает органы, подвергающиеся сильному растяжению, например, мочевыводящую систему. Западная медицина использует более подробную классификацию эпителия (см. Epithelium).
Самая распространенная и активно исследуемая форма метаплазии в организме — это Барреттов пищевод (синдром Барретта). Это опасное осложнение рефлюксной болезни, при котором содержимое желудка в пищеводе заменяет многослойный плоский эпителий, характерный для нормального пищевода, цилиндрическим (характерным для желудка) с примесью бокаловидных клеток, которые выделяют увлажняющую слизь (см. рис. 1).
Частота встречаемости данного синдрома при рефлюксе составляет 10%, а в общем населении — 1%. За последние 40 лет частота возникновения Барретта пищевода почти в 8 раз увеличилась. Он считается предраковым состоянием, так как аденокарцинома нижней части пищевода возникает при наличии данного синдрома в 10 раз чаще, чем при нормальном состоянии пищевода.
Неоднакратно исследовавшийся с момента первого описания в 1950 году синдром Барретта все еще имел некоторые неясные процессы развития, которые требовали выяснения: механизм возникновения метаплазии, при которой плоский эпителий заменяется цилиндрическим, происходит от каких клеток образующийся цилиндрический эпителий пищевода, как происходит последующая превращение в злокачественные опухоли?
Для пояснения процесса метаплазии было предложено пять основных теорий (они визуализированы на рисунке 2): 1) возможно, происходит прямое превращение плоского эпителия в цилиндрический — повреждение может вызвать переход одного типа ткани в другой (рисунок 2, a); 2) предшественниками цилиндрического эпителия могут быть циркулирующие в крови стволовые клетки, способные дифференцироваться в цилиндрический эпителий (рисунок 2, b); 3) предшественниками цилиндрического эпителия являются клетки субмукозных (слизистых) желез, находящихся под плоским эпителием (рисунок 2, c); 4) возможно, происходит экспансия крайних клеток цилиндрического эпителия желудка (рисунок 2, d); 5) предшественниками цилиндрического эпителия могут быть остаточные эмбриональные клетки, находящиеся вблизи границы (рисунок 2, e).

В научной литературе приведены несколько гипотез относительно возникновения пищевода Барретта. Ранее были предложены следующие предположения: а) передифференцировка плоского эпителия пищевода; б) дифференцировка стволовых клеток костного мозга, циркулирующих в крови; в) расширение и трансформация клеток слизистых желез пищевода в эпителий Барретта; г) превращение стволовых клеток слизистых желез; д) расширение и дифференцировка спящих остаточных эмбриональных клеток в пограничной области пищевода/желудка. Описанные гипотезы приведены на рисунке 2, который позаимствован из обсуждаемой статьи в журнале Nature.
Тем не менее, ни одна из этих теорий не была достаточно подтверждена экспериментально. Ни одна из этих гипотез не объясняет появления бокаловидных клеток, которые характерны для кишечника, а не для пищевода или желудка.
Исследование, выполненное группой ученых из Медицинского центра Колумбийского университета и других научных учреждений США и Китая, провело сравнительный анализ экспрессии генов, характерных для эпителия. Результаты показали, что в пограничном эпителии мышей, который состоит из базальных и люминальных клеток, имеется различная экспрессия трех маркеров в этих клетках.
В базальных клетках происходит экспрессия двух цитокератинов — Krt5 и Krt7, а также фактора регуляции транскрипции р63. В клетках люминального слоя происходит экспрессия только Krt7. Это является отличительной особенностью пограничной области от области пищевода, расположенной выше, где нет экспрессии Krt7 ни в базальных клетках, ни в плоском эпителии (рис. 1). В эпителии желудка ни один из этих маркеров не проявляет экспрессию.

Рисунок 3. Иллюстрация процедуры анастомоза между двенадцатиперстной кишкой и пищеводом у мышей, что приводит к поступлению желчных кислот (красные стрелки) в пищевод. Изображение взято из статьи, опубликованной в журнале Nature
В последующей серии экспериментов исследователи провели сложную хирургическую операцию на мышах, устанавливая соединение между пищеводом и двенадцатиперстной кишкой (рис. 3). В результате этого процесса желчные кислоты начали поступать в пищевод, имитируя рефлюкс.
Через 18 недель после операции, воздействие желчных кислот на границу между пищеводом и желудком привело к появлению клеток, называемых «пищеводом Барретта». В этих клетках был обнаружен характерный маркер CDX2, и они приобрели бокаловидную форму. Заинтересовавшим обстоятельством является то, что в верхней части пищевода наблюдение таких клеток не происходило, несмотря на то, что и она подвергалась воздействию желчных кислот.
Ученые приняли решение исключить возможность замещения эпителия в граничной области пищевода мигрирующими клетками соседних тканей. Для этого, с использованием генно-инженерных методов, они создали мышей, у которых в клетках эпителия граничной области происходила экспрессия гена Krt7, совмещенного с экспрессией красного флюоресцирующего белка Tomato.
Проведенные эксперименты показали, что клетки цилиндрического эпителия, известного как «пищевод Барретта», выражают Tomato, а значит, также экспрессируют ген Krt7. Как упоминалось ранее, ген Krt7 экспрессируется только в эпителии граничной области, но не в области пищевода выше и в желудке. Следовательно, клетки цилиндрического эпителия «пищевода Барретта» происходят исключительно от базальных клеток граничной области (рис. 4).

Иллюстрация 4. Предшественники базальных клеток (генетически обозначенные как p63 и KRT7) и люминальные клетки (KRT7 +) эпителия границы пищевода и желудка у мышей. Плоский эпителий пищевода — squamous epithelium. Эпителий границы пищевода — transitional epithelium. Желудок — cardia. Иллюстрация взята из статьи, обсуждаемой в журнале Nature.
В результате исследования, авторы решили определить, насколько схожа структура границы между пищеводом и желудком у человека и мыши. Они провели анализ экспрессии эпителиальных маркеров у человека и показали их сходство с мышиной структурой. В этой области у человека были выявлены базальные клетки, которые экспрессировали гены p63, KRT5 и KRT7, а также люминальные клетки, в которых проявлялся ген KRT7, но ген p63 не экспрессировался. В базальных клетках, принадлежащих области пищевода выше, ген KRT7 не проявлялся (иллюстрация 5).


Иллюстрация 5. В области перехода между пищеводом и желудком человека находится специфический эпителий, который атрофируется при развитии пищеводного Барретта. а — микроскопическое изображение предшественников базальных клеток (указаны стрелками) и клеток эпителия, окрашено гематоксилином и эозином. Длина шкалы — 50 мкм.
b — базальные клетки в пограничной области эпителия экспрессируют гены p63, KRT5 и KRT7 (экспрессируемые продукты обозначены треугольниками). Базальные клетки плоского эпителия пищевода не экспрессируют KRT7 (обозначены стрелками). Иммуногистохимическое окрашивание различными флуоресцентными красителями. Длина шкалы — 50 мкм. с — схема структуры пищеводно-желудочного эпителия человека, обозначения аналогичны рисунку 4. Рисунок из рассматриваемой публикации в журнале Nature
С применением проточной цитометрии произведено разделение двух видов базальных клеток пищевода человека (с маркерами p63 + KRT7 − и p63 + KRT7 + ). Из этих клеток in vitro получены трехмерные культуры органоидов, и обнаружено, что органоиды, полученные из клеток типа p63 + KRT7 + , принадлежащих границе пищевода, могут формировать эпителиальные клетки, аналогичные эпителию кишечника. Органоиды, полученные из клеток типа p63 + KRT7 − , взятых из верхней области, не обладают такой способностью.
Таким образом, экспериментальным исследованиям удалось изучить эпителий, расположенный на границе между пищеводом и желудком, на моделях лабораторных мышей. Этот эпителий является источником патологического состояния — пищевода Барретта. Было установлено, что данный эпителий является более чувствительным к разрушительным факторам, чем эпителий вышележащих областей пищевода или эпителий желудка. Полученные результаты подтверждают предположение о том, что базальные клетки пограничного эпителия могут превращаться в кишечный эпителий, включая бокаловидные клетки.
В то же время обнаруженные в ходе исследования генетические индикаторы эпителиальных клеток пограничной зоны маловероятно могут быть инициатором формирования пищевода Барретта и последующего развития рака. Вероятнее всего, здесь имеются в виду другие факторы, такие как кислотный рефлюкс, другие химические раздражители, нарушения гормонального баланса или вирусные инфекции.
Несмотря на остающиеся вопросы, исследование, которое обсуждается, представляет подробную картину формирования пищевода Барретта. Поскольку предраковые состояния и злокачественные опухоли особенно часто возникают в границах эпителия различных органов (матка, пищевод, прямая кишка), можно предположить, что здесь действуют аналогичные механизмы.
Кроме того, будущие исследования должны разъяснить данный вопрос, а также определить, является ли пограничный эпителий единственным местом возникновения этой метаплазии и последующего ее превращения в рак. Действительно, давно было доказано, что структура, аналогичная пищеводу Барретта, может возникнуть у пациентов, у которых граница пищевода была удалена (С. Р. Хамильтон, Дж. Х. Ярдли, 1977. Регенерация слизистой оболочки сердечного типа и приобретение слизистой оболочки Барретта после эзофагогастростомии). Таким образом, полученные результаты могут способствовать разработке методов диагностики, профилактики и лечения этих состояний не только в отношении пищевода, но и других органов.
