Паракератоз пищевода — это патологическое состояние, характеризующееся нарушением нормальной функции клеток эпителия пищевода, что ведет к увеличению количества кератинизированных клеток на поверхности слизистой. Этот процесс может быть следствием хронического воспаления, рефлюксной болезни или других заболеваний, что требует тщательной диагностики.
Лечение паракератоза зависит от основной причины его возникновения. Важно обеспечить контроль за факторами, способствующими этому состоянию, что может включать изменения в диете и образе жизни, а также применение медикаментов, направленных на снижение воспаления и нормализацию состояния слизистой. В некоторых случаях может потребоваться хирургическое вмешательство.
- Паракератоз пищевода — это паталогическое изменение эпителия, характеризующееся его ороговением.
- Основные причины паракератоза включают хронические воспалительные процессы, рефлюкс-страдания и травмы.
- Симптомы могут включать дискомфорт в области глотки, трудности при глотании и болевые ощущения за грудиной.
- Диагностика основывается на гастроскопии и биопсии, что позволяет определить степень изменений.
- Лечение направлено на устранение первопричины, может включать медикаментозную терапию и изменение образа жизни.
- При своевременной diagnosis и лечении прогноз обычно благоприятный.
Эрозия пищевода
Эрозия пищевода — это заболевание, заключающееся в образовании дефектов на слизистой оболочке пищевода. Она проявляется как единичными, так и множественными участками поражения, чаще всего в нижней трети органа. Основные симптомы включают изжогу, дискомфорт за грудиной, затруднения при глотании, отрыжку, утренние приступы тошноты и метеоризм.
Для диагностики применяется комплексный подход, который включает сбор анамнеза, эндоскопическое исследование пищевода, рентгенографические методы и лабораторные анализы. Лечение предполагает соблюдение специальной диеты и прием медикаментов, направленных на нейтрализацию соляной кислоты. Если консервативная терапия не дает результатов или возникают осложнения, может потребоваться хирургическое вмешательство.
- По происхождению: первичные — возникают под воздействием соляной кислоты; вторичные — развиваются как осложнения различных заболеваний;
- По количеству эрозий: одиночные и множественные;
- По характеру течения: острые — наблюдаются в течение 1-8 недель; хронические — фиксируются более 5 лет.
Причины эрозии пищевода
Чаще всего эрозивное поражение пищевода связывают с недостаточностью запирательного аппарата пищевода. Это клапан, который пропускает в пищевод заглатываемую пищу и одновременно препятствует забросу соляной кислоты желудка. При недостаточности замыкающего сфинктера происходит его самопроизвольное открытие, и соляная кислота из желудка попадает в пищевод. В результате длительного контакта желудочного сока с эпителием пищевода образуются очаги эрозии, и даже глубокие язвенные дефекты.
Недостаточность пищеводного замыкающего устройства может возникать по разным причинам:
- неконтролируемый прием некоторых медикаментов,
- зависимость от наркотиков,
- курение,
- избыточное употребление цитрусовых и кофе,
- ненормированный и обильный прием пищи,
- неправильное опорожнение желудка,
- расстройства перистальтики кишечника,
- гастроэзофагеальная рефлюксная болезнь.
Формирование эрозии пищевода связано с повышенным давлением внутри желудка и брюшной полости. Подобные патологии могут наблюдаться при ожирении, метеоризме и новообразованиях в брюшной полости. Давление в желудке часто повышается во время беременности, при наклонах корпуса и после обильной еды в положении лежа.
Выброс агрессивного желудочного содержимого в пищевод инициирует и поддерживает грыжа пищеводного отверстия диафрагмы. Это смещение части желудка, пищевода и кишечника в грудную полость. Патология бывает врожденная и приобретенная, и связана с укорочением пищевода, ослаблением связочного аппарата диафрагмы, искривлением позвоночника в грудном отделе.
Риск эрозивных поражений пищевода увеличивается под воздействием ряда факторов:
- недостаток витаминов,
- хронические заболевания,
- ослабленный иммунитет,
- пожилой возраст,
- воздействие химикатов,
- частый прием горячих напитков,
- психоэмоциональные и физические нагрузки.
Эрозия пищевода чаще наблюдается у пациентов с сопутствующими заболеваниями органов пищеварения, такими как гастрит, язва желудка, дуоденит и бульбит.
У детей младше года эрозия пищевода встречается крайне редко и обычно связана с заболеваниями пищеварительного тракта, недостаточно развитой слизистой оболочкой и запирательным аппаратом пищевода. В анамнезе таких пациентов могут встречаться неблагоприятные перинатальные обстоятельства — гипоксия, родовые травмы, недоношенность и повреждения центральной нервной системы.
Справка! Употребление продуктов, не соответствующих возрасту младенца, провоцирует задержку пищевых масс в желудке, повышение внутрибрюшного давления, которое является фактором риска эрозии.
Паракератоз пищевода – это патологическое состояние, характеризующееся изменением эпителия пищевода. При этом процессе происходит утолщение рогового слоя эпителия, что может быть вызвано различными факторами, включая раздражение, воспаление и хронические заболевания. Данная патология может сопровождаться такими симптомами, как дисфагия, жжение и дискомфорт в области груди. Неконтролируемое развитие паракератоза может привести к более серьезным заболеваниям, таким как дисплазия или рак пищевода.
Лечение паракератоза пищевода, как правило, зависит от причины, вызвавшей это состояние. На первом этапе необходимо выявить и устранить основное заболевание или фактор, способствующий изменениям в слизистой оболочке. В некоторых случаях может потребоваться медикаментозная терапия, включая использование противовоспалительных и цитопротекторных средств для восстановления нормального эпителия. Важным аспектом является также соблюдение диеты, избегание острого и раздражающего питания, а также контроль за состоянием пищевода со стороны гастроэнтеролога.
Кроме того, важно регулярно проходить обследования, чтобы оценить динамику состояния пищевода и предотвратить осложнения. Необходимо обращать внимание на дополнительные симптомы, которые могут указывать на прогрессирование заболевания. В случае появления тревожных признаков, таких как сильная боль в груди или значительное ухудшение состояния, необходимо незамедлительно обратиться к специалисту для более глубокого обследования и коррекции лечения.
Формы пищевода Баррета
Выделяют следующие морфологические варианты пищевода Барретта:
- Кардиальный тип. Находится в форме ямок (фовеолярная поверхность) и включает муцинпродуцирующие элементы.
- Фундальный тип. В этом случае, кроме муцинпродуцирующих клеток, присутствуют клетки, характерные для желудочного эпителия — главные и обкладочные клетки.
- Цилиндроклеточный тип. Гистологически напоминает кишечный эпителий, так как образует складки и содержит бокаловидные клетки наряду с муцинпродуцирующими клетками.
Именно цилиндроклеточный тип наиболее подвержен диспластическим трансформациям и развитию рака. По этой причине многие специалисты предлагают рассматривать пищевод Барретта как метаплазию только с наличием бокаловидных клеток.
Кроме того, заболевание классифицируется в зависимости от протяженности измененного участка. Здесь различают короткий пищевод Барретта, когда длина измененного участка не превышает 3 см, и длинный ПБ — превышающий в размерах 3 см.
Причины
Основной причиной метаплазии пищевода является гастроэзофагеальный рефлюкс — заброс содержимого желудка в пищевод. В этом случае агрессивный желудочный сок вызывает раздражение слизистой, что приводит к замещению многослойного плоского эпителия на более устойчивый к агрессивному воздействию цилиндрический эпителий, что и называется метаплазией — заменой одного типа ткани другим. Постоянное раздражение приводит к тому, что метаплазированный эпителий создает клон клеток с нарушениями анонсированной гибели (апоптоза). Это состояние называется дисплазией и впоследствии может перейти в рак.
Дополнительными факторами риска являются:
- Пищеводно-диафрагмальные грыжи, способствующие постоянному смещению желудка и, следовательно, постоянному рефлюксу.
- Ожирение.Во-первых, ожирение способствует повышению внутрибрюшного давления, что вызывает рефлюкс. Во-вторых, в этом состоянии увеличивается объем околопищеводной клетчатки, которая выделяет провоспалительные цитокины, оказывающие негативное влияние на слизистую пищевода.
- Курение.
- Метаболический синдром.
Предрак пищевода
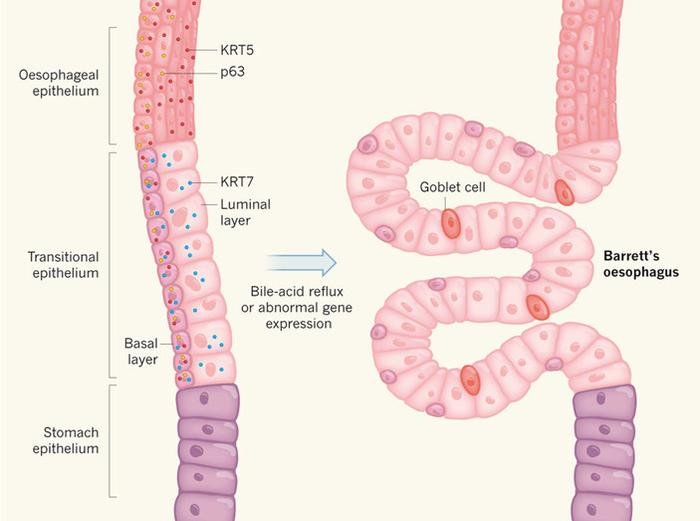
Рис. 1. Схематическое изображение эпителия в месте сочленения пищевода (Oesophagus) и желудка (Stomach), в котором встречаются эпителиальные клетки разных типов. Переходный эпителий (Transitional epithelium) образован базальными (Basal layer) и люминальными (Luminal layer) клетками, которые характеризуются различным уровнем экспрессии трех белков-маркеров (p63, KRT5 и KRT7). Рефлюкс, вызванный желчными кислотами, или нарушение экспрессии каких-то генов могут вызвать превращение эпителия пограничной области в аномальный – подобный эпителию кишечника – с включениями бокаловидных клеток (Goblet cell), и формируется разрастающаяся структура, называемая пищеводом Барретта (Barrett’s oesophagus). Рисунок из популярного синопсиса к обсуждаемой статье.
Ученые смогли разгадать механизм развития предракового состояния на границе между пищеводом и желудком — синдрома Барретта. Они смогли детально охарактеризовать эпителий в этой переходной зоне и на лабораторных животных продемонстрировали, что базальные клетки с определенным набором маркеров могут стать предшественниками тканей, схожих с кишечными, которые заменяют нормальный эпителий данной области. Аналогичные клетки были найдены на границе пищевода и желудка и у людей, и это исследование должно поспособствовать улучшению методов ранней диагностики и терапии онкологического заболевания.
Хорошо известно, что чем раньше диагностировать и начать лечить рак, тем легче может быть само лечение и тем выше шансы на выздоровление. Для некоторых типов рака выявлены так называемые предраковые состояния – изменения тканей, которые сами по себе не являются злокачественными, но повышают вероятность развития рака в этих тканях. Такие состояния известны пока для относительно небольшого числа раков. Поэтому, с одной стороны, нужно пытаться расширять список соответствий между злокачественными опухолями и предраковыми состояниями, а с другой стороны – выяснять механизмы возникновения этих состояний, чтобы повышать эффективность профилактики рака.
Одним из типов предраковых состояний являются метаплазии, когда происходит замена клеток одного типа на клетки другого (обычно обратимого). Метаплазии часто возникают по границам между различными типами эпителия и в некоторых случаях могут приводить к развитию карцином — злокачественных опухолей эпителиального происхождения.
Эпителий – это ткань, выстилающая поверхность тела (то есть, грубо говоря, кожа), внутренние полости и слизистые оболочки органов. В российской медицине различают два основных вида эпителия – многослойный плоский эпителий (кожа, слизистые оболочки, пищевод) и однослойный цилиндрический эпителий (желудок, кишечник). Особо выделяют эпителий, выстилающий органы, подвергающиеся сильному растяжению (например, в мочевыводящей системе), так называемый переходный. В западной медицине принята более детальная классификация эпителия (см. Epithelium).
Наиболее часто исследуемой и распространенной формой метаплазии является синдром Барретта (пищевод Барретта). Это серьезное осложнение, возникающее при рефлюксной болезни, которая характеризуется забросом желудочного содержания в пищевод. При этом в области соединения пищевода и желудка многослойный плоский эпителий, нормальный для пищевода, заменяется на цилиндрический эпителий, присущий желудку. Этот эпителий также содержит бокаловидные клетки, характерные для кишечника, которые выделяют смазочную слизь (см. рис.
1). Частота встречаемости синдрома при рефлюксе составляет 10%, а в целом по популяции – 1%. За последние 40 лет частота встречаемости пищевода Барретта возросла почти в 8 раз. Он считается предраковым состоянием, так как высоколетальная аденокарцинома нижней части пищевода возникает при нем в 10 раз чаще, чем в нормальном пищеводе.
С момента первого описания синдрома Барретта в 1950 году его изучение активно продолжалось, однако ключевые механизмы его формирования оставались без ответа: как происходит замещение плоского эпителия цилиндрическим? От каких клеток возникает этот новый цилиндрический эпителий в пищеводе? Как далее развиваются злокачественные образования?
Для объяснения метаплазии было предложено пять основных теорий (они схематично показаны на рис. 2):
1) Вариант предполагает прямую трансформацию плоского эпителия в цилиндрический – повреждение ткани может привести к ее изменению (рис. 2, a);
2) предшественниками цилиндрического эпителия являются циркулирующие в кровотоке стволовые клетки, способные дифференцироваться в цилиндрический эпителий (рис. 2, b);
3) Предшественниками цилиндрического эпителия могут быть клетки подслизистых (слизистых) желез, находящихся под плоским эпителием (рис. 2, c);
4) возможно экспансия в пограничную область клеток цилиндрического эпителия желудка (рис. 2, d);
5) Возможными предшественниками также являются остаточные эмбриональные клетки, находящиеся в области стыка (рис. 2, e).
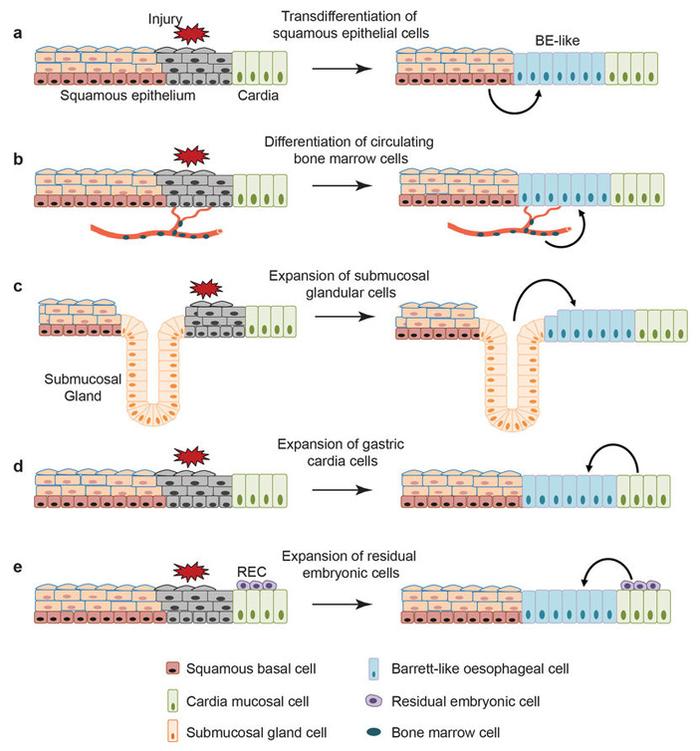
Рис. 2. Гипотезы возникновения пищевода Барретта, предложенные ранее. a – передифференцировка плоского эпителия пищевода; b – дифференцировка циркулирующих в крови стволовых клеток костного мозга; c – экспансия клеток слизистых желез пищевода и их превращение в эпителий Барретта; d – превращение стволовых клеток слизистых желез; e – экспансия и дифференцировка спящих остаточных эмбриональных клеток пограничной области пищевода/желудка. Рисунок из обсуждаемой статьи в Nature
Тем не менее, ни одна из этих гипотез не получила подтверждения в экспериментах и ни одна не объясняла возникновения кишечных бокаловидных клеток в эпителии (в отличие от клеток пищевода и желудка).
Большой коллектив ученых из Медицинского центра Колумбийского университета и других научных учреждений США и Китая провел сравнительный анализ экспрессии генов, характерных для эпителия. Они показали, что у мышей пограничный эпителий, состоящий из базальных и люминальных (обращенных в просвет пищевода) клеток, характеризуется различной экспрессией в этих клетках трех маркеров.
В базальных клетках наблюдается экспрессия двух цитокератинов – Krt5 и Krt7, а также регуляторного фактора транскрипции р63. В клетках люминального слоя выявляется только Krt7. Это отличие позволяет отделить пограничную область от верхней части пищевода, где ни в базальных клетках, ни в плоском эпителии Krt7 не экспрессируется (рис. 1). В эпителии желудка ни один из этих маркеров не наблюдается.
В следующей серии экспериментов авторы провели тонкую хирургическую операцию на мышах и сделали анастомоз между пищеводом и двенадцатиперстной кишкой (рис. 3).
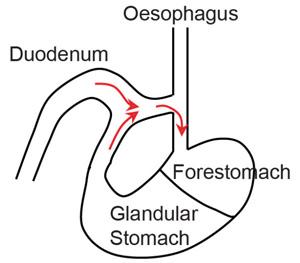
Рис. 3. Иллюстрация анастомоза между двенадцатиперстной кишкой и пищеводом мыши, приводящего к тому, что желчные кислоты (красные стрелки) проникают в пищевод. Иллюстрация из обсуждаемой статьи в Nature.
В результате желчные кислоты поступали в пищевод, что позволило имитировать рефлюкс.
Спустя 18 недель после процедуры, воздействие желчных кислот на пограничную область способствовало формированию клеток «пищевода Барретта», в которых проявлялся характерный маркер CDX2, и там начали появляться бокаловидные клетки. Примечательно, что в верхней части пищевода подобных клеток не обнаружилось, даже несмотря на их контакт с желчными кислотами.
Ученые решили исключить возможность замещения эпителия в пограничной области пищевода мигрирующими клетками соседних тканей. Для этого с помощью генно-инженерных методов они получили мышей, у которых экспрессия гена Krt7в клетках эпителия пограничной области была сопряжена с экспрессией красного флюоресцирующего белка Tomato.
Экспериментальные данные показали, что в клетках цилиндрического эпителия «пищевода Барретта» экспрессируется Tomato, что соответствует Krt7. Упомянутый ген Krt7 активен в пограничном эпителии, но не проявляется в верхних участках пищевода и в желудке. Это указывает на то, что цилиндрический эпителий «пищевода Барретта» формируется исключительно из базальных клеток пограничной области (рис. 4).
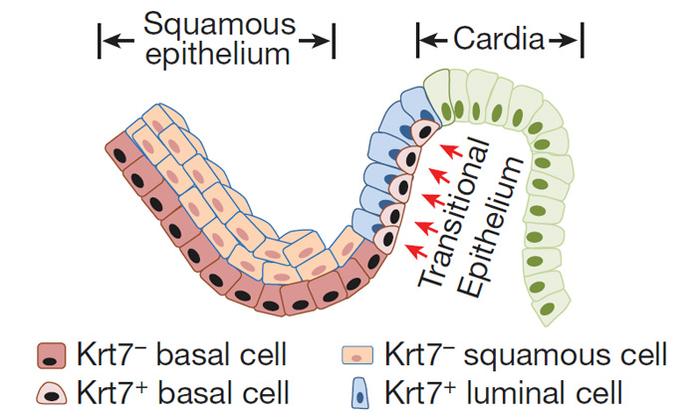
Рис. 4. Предшественники базальных клеток (экспрессирующие гены p63 и KRT7) и люминальные клетки (KRT7+) эпителия пограничной области пищевод/желудок у мышей. Squamous epithelium – плоский эпителий пищевода. Transitional epithelium – эпителий пограничной области пищевода. Cardia – желудок. Рисунок из обсуждаемой статьи в Nature
В конечном итоге авторы работы решили оценить структурные сходства между пограничной областью пищевода и желудка у людей и мышей. Проведенный анализ экспертной экспрессии указал на их схожесть. У человека в этой области были обнаружены базальные клетки с экспрессией генов p63, KRT5 и KRT7, а также люминальные клетки с проявлением KRT7, без экспрессии p63. В находящихся выше базальных клетках пищевода KRT7 не выявлялся (рис. 5).
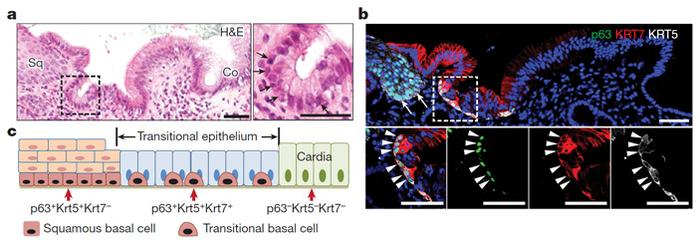
Рис. 5. В пограничной области пищевода и желудка человека локализован специфический переходный эпителий, который разрастается при пищеводе Барретта. a – микроскопическое изображение предшественников базальных клеток (отмечены стрелками) и люминальных клеток эпителия, окраска гематоксилином и эозином.
Ширина изучаемого участка составила 50 мкм. b – базальные клетки пограничного эпителия демонстрируют экспрессию генов p63, KRT5 и KRT7 (отрезки экспрессии выделены треугольниками). В базальных клетках плоского эпителия пищевода KRT7 не имеется (показано стрелками). Исследование проводилось с применением различных флюоресцентных красителей. Ширина изучаемого участка составила 50 мкм. c – схема строения эпителия в пограничной области между пищеводом и желудком человека, с обозначениями, аналогичными рис. 4. Схема из статьи в Nature.
С помощью проточной цитометрии были разделены два типа базальных клеток пищевода человека (с маркерами p63+KRT7− и p63+KRT7+). Из этих клеток in vitro были получены трехмерные культуры органоидов и оказалось, что органоиды, полученные из клеток типа p63+KRT7+ и происходящие из пограничной области пищевода, способны формировать эпителиальные клетки, подобные эпителию кишечника. Органоиды, полученные из клеток типа p63+KRT7−, взятых из выше расположенной области, таким свойством не обладали.
Таким образом, исследователи на модели лабораторных мышей выявили свойства пограничного эпителия между пищеводом и желудком, который потенциально может привести к предраковому состоянию – пищеводу Барретта. Также они подтвердили, что строение у людей аналогично. Выяснилось, что этот эпителий демонстрирует большую восприимчивость к повреждающим воздействиям по сравнению с эпителием, расположенным выше в пищеводе, или эпителием желудка. Результаты согласуются с ранее выдвинутыми гипотезами о происхождении пищевода Барретта, а именно о прямой трансформации клеток пограничной области в подобные кишечным: была продемонстрирована возможность базальных клеток пограничного эпителия становиться предшественниками эпителия с кишечным типом строения, включая бокаловидные клетки.
В то же время выявленные в ходе исследования генетические маркеры клеток эпителия пограничной зоны как таковые вряд ли могут быть причиной формирования пищевода Барретта и дальнейшего развития рака. В этом, скорее всего, задействованы какие-то иные факторы – кислотный рефлюкс, другие химические раздражители, гормональные нарушения или вирусные инфекции.
Несмотря на наличие нерешенных вопросов, данная работа предоставляет подробное понимание процессов формирования пищевода Барретта. Поскольку предраковые состояния и злокачественные опухоли часто появляются именно в пограничных слоях эпителия различных органов (матка, пищевод, прямая кишка), можно надеяться на существование схожих механизмов в этих случаях.
Впрочем, дальнейшие исследования должны будут прояснить этот вопрос, равно как и то, является ли пограничный эпителий единственным местом возникновения этой метаплазии и дальнейшей трансформации ее в рак. Ведь уже давно было показано, что структура, подобная пищеводу Барретта, может возникнуть и у больных, у которых пограничная область пищевода была удалена (S. R. Hamilton, J. H. Yardley, 1977. Regnerative of cardiac type mucosa and acquisition of Barrett mucosa after esophagogastrostomy). Так что полученные результаты могут способствовать разработке методов диагностики, профилактики и лечения этих состояний не только применительно к пищеводу, но и к другим органам.
- профилактика рака
- ранняя диагностика
- биомаркеры
Вы еще никогда так не уставали
Образ жизни затрагивает каждого из нас, будь то аллергия или мигрень, может вызвать постоянную усталость. Если состояния усугубляются и проявляются дополнительные симптомы, это может оказаться раком пищевода. Однако диагноз должен подтвердить врач, поэтому рекомендуется как можно скорее обратиться к специалисту, так как лечение рака пищевода наиболее эффективно на стадиях 1, 2 и 3 без применения химической терапии.
Питание и образ жизни играют большую роль в профилактике рака пищевода. Самыми большими факторами риска являются курение, алкоголь и ароматизированные продукты. Люди, употребляющие алкоголь и курящие, гораздо больше подвержены риску рака пищевода. Люди с диагнозом пищевод Барретта имеют повышенный риск развития рака пищевода, поэтому регулярные медицинские осмотры очень важны и обязательны для профилактики.
Правильное питание – один из способов снизить риск рака пищевода. Важно ежедневно употреблять фрукты и овощи, избегать очень горячих напитков, а людям с диагнозом рефлюкс желудка следует регулярно проходить медицинское обследование.
Осложнения кандидоза пищевода
При кандидозе пищевода возможно кровотечение, которое возникает при травмировании слизистой оболочки пищей. Есть риск железодефицитной анемии.
В крайне редких случаях воспаление может распространяться, приводя к грибковой инфекции других внутренних органов.
Диагностика кандидоза пищевода
Диагностика проводится в несколько этапов.
В первую очередь проводится эзофагогастроскопия – эндоскопическое исследование верхних отделов желудочно-кишечного тракта с помощью зонда, оснащенного камерой. В ходе процедуры врач может взять образцы пораженных участков слизистой оболочки для дальнейших лабораторных анализов.

Во время эзофагогастроскопии поверхность ЖКТ исследуют с помощью зонда
Для определения типа возбудителя проводят посев налета из пищевода. Также исследуется материал на чувствительность к противогрибковым препаратам, что необходимо для назначения эффективного лечения.
Паракератоз пищевода что это значит и как лечить
- ГлавнаяЛапароскопическая хирургия
- Гастроэзофагальная рефлюксная болезнь (ГЭРБ)
- Пищевод Баррета, дисплазия и рак пищевода
Самое серьезное осложнение ГЭРБ – это пищевод Баррета, метаплазия, представляющая собой фактор, который увеличивает риск развития рака пищевода (аденокарциномы). Изменение клеток слизистой оболочки при пищеводе Баррета представляет собой кишечную метаплазию, при которой обычные клетки слизистой пищевода заменяются клетками, характерными для кишечной стенки.
Кишечная метаплазия может перейти в дисплазию (метаплазия и дисплазия – последовательные по нарастающей тяжести изменений процессы перерождения клеток) и затем развиться в злокачественную опухоль. Поэтому метаплазия Баррета является предраковым состоянием, хотя рак пищевода – довольно редкое заболевание, больше распространенное среди мужчин. Распространенность пищевода Баррета среди взрослого населения составляет 8-10%.
Ожирение также является независимым фактором риска для возникновения аденокарциномы пищевода, а в сочетании с рефлюксной болезнью оно значительно увеличивает этот риск. Однако общий риск развития аденокарциномы остается достаточно низким даже у пациентов с выраженными симптомами рефлюкса.
В зависимости от участка пищевода, где развивается метаплазия Баррета (и затем, возможно, аденокарцинома), специалисты разделяют это заболевание на три типа: метаплазия в области длинного сегмента пищевода, метаплазия в области короткого сегмента пищевода (в 3 см и менее от места перехода пищевода в желудок) и метаплазия в области кардиальной части желудка (часть желудка, расположенная сразу после перехода пищевода в желудок).
По результатам эндоскопических исследований распространенность метаплазии Баррета в длинном сегменте пищевода составляет около 1%. Этот показатель увеличивается с усугублением ГЭРБ. Данная форма метаплазии чаще встречается у лиц в возрасте от 55 до 65 лет, и намного чаще у мужчин (отношение мужчин и женщин 10:1).
Метаплазия Баррета в области короткого сегмента встречается чаще, однако, распространенность этого заболевания оценить сложно, так как этот тип метаплазии при эндоскопическом исследовании сложно отличить от метаплазии в кардиальном отделе желудка. При этом злокачественная опухоль при метаплазии в области короткого сегмента пищевода и кардиальной части желудка развивается реже, чем при метаплазии в области длинного сегмента пищевода.
Несмотря на то, что метаплазия Баррета в пищеводе явно возникает на фоне гастроэзофагеальной рефлюксной болезни (ГЭРБ) и иногда перерастает в рак пищевода, причины превращения клеток в кишечную метаплазию в кардиальной части желудка остаются неясными. Этот вид метаплазии наблюдается как при ГЭРБ, так и при гастрите, вызванном инфекцией Helicobacter pylori. Исследования показывают, что метаплазия в области кардиального отдела желудка чаще развивается на фоне гастрита, чем на фоне ГЭРБ. Однако кишечная метаплазия и воспаление могут возникнуть и при отсутствии Helicobacter pylori, и тогда это является следствием хронического рефлюкса. Примерно 1,4% населения страдает от данного типа метаплазии.
Хотя непосредственная причина метаплазии Баррета остается неясной, тем не менее, очевидным является тот факт, что метаплазия развивается на фоне ГЭРБ и связана с чрезмерным патологическим воздействием кислоты на слизистую оболочку пищевода. Исследования с использованием рН-мониторирования показали, что у пациентов с метаплазией Баррета значительно увеличена частота рефлюксов и продолжительность пищеводного клиренса. Это может быть связано с выраженным нарушением сократительной функции мышц пищевода, развивающимся вследствие тяжелого эзофагита. Кроме того, у большинства пациентов с тяжелым эзофагитом имеется грыжа пищеводного отверстия диафрагмы.
Кроме того, манометрия длинного сегмента пищевода у пациентов с метаплазией Баррета указывает на пониженный тонус нижнего пищеводного сфинктера и нарушения перистальтики, которые напоминают таковые при тяжелом эзофагите. Остается вопросом, почему одни пациенты с тяжелым эзофагитом имеют метаплазию Баррета, а другие — нет. В этом контексте допускается, что генетическая предрасположенность играет определенную роль.
Пищевод Баррета — Наблюдение и лечение
В лечении пациентов с пищеводом Баррета акцент делается на два аспекта: коррекцию ГЭРБ, способствующей развитию метаплазии, и предупреждение рака пищевода. Методика лечения эзофагита и метаплазии Баррета аналогична таковой при обычной ГЭРБ, с учетом более выраженного влияния кислоты на слизистую оболочку пищевода, что требует более агрессивной терапии. Обычно назначают ингибиторы протонной помпы, но в случаях неэффективности может потребоваться хирургическое вмешательство.
Некоторые специалисты, основываясь на данных исследований, которые показали, что клеточные изменения происходят именно за счет патологического воздействия кислоты на слизистую оболочку желудка, предлагают использовать для лечения пищевода Баррета препараты, подавляющие секрецию соляной кислоты в желудке. Однако клинически не доказано, что применение антисекреторных препаратов или антирефлюксная операция могут предотвратить развитие аденокарциномы пищевода или привести к обратному развитию кишечной метаплазии. Таким образом, основной целью лечения является терапия эзофагита..
Поскольку на сегодняшний день не найдены пути предотвращения метаплазии Баррета, основными задачами врача являются минимизация риска рака пищевода. В этой связи пациенты с данным состоянием проходят регулярное эндоскопическое обследование с обязательной биопсией для оценки степени клеточной метаплазии или дисплазии в слизистой пищевода.
Сроки обследования устанавливаются в зависимости от тяжести имеющихся изменений слизистой оболочки пищевода. Так пациенты, у которых имеется только метаплазия Баррета без дисплазии, проходят обследование один раз в 2-3 года.
В случае обнаружения дисплазии проводится углубленное обследование для определения ее степени, так как высокоградусная дисплазия может привести к онкологическому заболеванию в течение 4 лет.
Пациентам с низкой степенью дисплазии назначается 12-недельный курс ингибиторов протонной помпы в высоких дозах, затем проводится повторное обследование с биопсией. Если обследование подтверждает наличие дисплазии низкой степени выраженности, то в последующем эндоскопия проводится через 6 месяцев, а затем ежегодно, если не отмечено развития дисплазии высокой степени.
Хирургические методы лечения пищевода Баррета
Хирургическое лечение пищевода Баррета направлено на снижение количества эпизодов рефлюкса.
Несмотря на то что рефлюксная болезнь увеличивает вероятность аденокарциномы пищевода, пока не ясно, является ли наличие пищевода Баррета прямой причиной его формирования, или же существуют другие факторы, способствующие злокачественным изменениям клеток.
Уменьшению симптомов заболевания способствует как медикаментозное, так и хирургическое лечение пищевода Баррета. Однако по данным исследований даже прием ингибиторов протонной помпы в больших дозах не способствует уменьшению частоты рефлюкса.
Поэтому, даже с улучшением состояния пациентов благодаря медикаментозному лечению, хирургические вмешательства в случае пищевода Баррета остаются значимыми. Данные некоторых исследований свидетельствуют о том, что после лапароскопической фундопликации риск онкологических заболеваний снижается по сравнению с медикаментозной терапией. Однако, после операции возрастает риск летальности, что связывают с неизвестными факторами, приводящими к повышению заболеваемости сердечно-сосудистыми недугами у таких пациентов. Следовательно, решение о хирургическом вмешательстве принимается врачом после тщательной оценки всех элементов “за” и “против”. В случае удачного вмешательства опытного хирурга результаты могут быть весьма положительными, хотя это не гарантирует полного исчезновения симптомов, что иногда требует послеоперационного применения препаратов.
Данные исследований показывают, что медикаментозная терапия, в отличие от хирургического лечения, оказывает меньший эффект на частоту возникновения рефлюкса во время сна. В этой ситуации достаточно эффективными оказываются как лапароскопическая, так и открытая операция.
Также, по некоторым данным, полученным в ходе длительных наблюдений, риск дисплазии и рака после фундопликации ниже, чем после консервативного лечения.
Хирургическое лечение рекомендуется также пациентам, с пищеводом Баррета в сочетании с наличием грыжи пищеводного отверстия диафрагмы.
Эндоскопическая абляция
Этот метод хирургического лечения пищевода Баррета сопряжен с меньшим риском развития осложнений, чем большая хирургическая операция. Теоретически, данный метод является относительно безопасным.
Суть операции заключается в удалении пораженной области слизистой оболочки пищевода. На этом месте происходит дальнейшее восстановление нормальной слизистой, что значительно снижает риск возникновения рака. Удаление осуществляется с помощью лазера или другого высокоэнергетического излучения. Пациентам также назначается прием ингибиторов протонной помпы в высоких дозах для содействия нормализации слизистой оболочки пищевода.
Операция проводится либо без подготовки, либо после приема специальных препаратов, воздействующих на клетки измененной части пищевода и подготавливающих к лазерному воздействию для улучшения результата операции.
Хирургическое лечение при высокой степени дисплазии
При дисплазии высокой степени риск развития аденокарциномы также становится высоким. Дисплазия может быть обнаружена только на одном участке слизистой оболочки пищевода (фокальная), а может развиться сразу в нескольких местах (мультифокальная), и такая дисплазия сочетается со значительным риском развития аденокарциномы (27% в течение 3 лет).
У больных с пищеводом Баррета, обладающими высокой степенью дисплазии, эндоскопическая абляция слизистой оболочки не всегда оправдана. Это связано с тем, что такой подход затрудняет полное удаление пораженной ткани, а высокий риск рака сохраняется, даже если имеется небольшой участок пораженных клеток. Поэтому можно проводить эндоскопическую операцию только при строгих показаниях, с тщательной оценкой возможных рисков.
Эндоскопическая абляция проводится у тех пациентов, которым не рекомендуется проведение эзофагэктомии (большая операция, при которой удаляется часть пищевода или весь пищевод). В остальных случаях предпочтительным методом хирургического лечения пищевода Баррета с высокой степенью дисплазии остается эзофагэктомия.
Эзофагэктомия является эффективным методом при лечении молодых и в целом здоровых пациентов, но сопряжена с заметным риском смертности (3-10%). По этой причине некоторые эксперты рекомендуют проводить регулярные (с высоким интервалом) эндоскопические наблюдения вместо немедленной операции в случае высокой степени дисплазии у больных с пищеводом Баррета.
Поскольку операция удаления пищевода сопряжена с высоким риском, в качестве альтернативного метода хирургического лечения пищевода Баррета с высокой степенью дисплазии применяется эндоскопическая абляция. Эта операция может проводиться термическим, химическим или механическим способом. В любом случае операция состоит в удалении метаплазированного или дисплазированного эпителия в сочетании с интенсивной антисекреторной терапией, что в последующем обуславливает восстановление нормального эпителия слизистой оболочки пищевода.
Эндоскопическая резекция слизистой оболочки пищевода
Это еще один метод хирургического лечения пищевода Баррета. Методика операции состоит в хирургическом иссечении пораженной части слизистой оболочки с помощью специальных эндоскопических инструментов, в том числе электрокоагулятора (который используется, например, при эндоскопическом удалении полипов).
Эффективность данной процедуры достаточно высока, однако рецидив заболевания может проявиться уже в первый год после операции.
Термическая абляция производится с помощью электрокоагулятора, аргонового плазменного коагулятора или лазерного облучения. Одним из осложнений данной операции является перфорация пищевода. Другой способ абляции – фотодинамическое облучение с помощью специального прибора.
Как и в случае термической абляции, данная методика может вызывать ряд побочных эффектов: болевые ощущения в груди, тошноту и стриктуры пищевода. Также пациентов следует предупредить о необходимости избегать длительного пребывания на солнце после операции, так как возможно возникновение повышенной чувствительности кожи к ультрафиолетовому излучению. Эта процедура очень эффективна и приводит к обратному развитию дисплазии у 90% пациентов. В то же время остаточные проявления метаплазии Баррета фиксируются в течение 2-62 месяцев у 58% прошедших фотодинамическую абляцию.
Механическая абляция заключается в механическом удалении измененной части слизистой оболочки пищевода с помощью специальных эндоскопических инструментов. Эта процедура рекомендуется тем пациентам, у которых наблюдается ранняя стадия развития рака пищевода и которым по тем или иным причинам не может быть проведена большая хирургическая операция (удаление пищевода).
Опыт других людей
Светлана, 35 лет, мама двоих детей: «У моего сына выявили паракератоз пищевода после проверки по поводу постоянных болей в животе. Мы сначала паниковали, но врач объяснил, что это состояние связано с изменениями в клетках пищевода, и не всегда означает серьезную патологию. Лечение заключалось в соблюдении диеты, исключении острых и раздражающих блюд. Также нам прописали медикаменты для снижения кислотности. После нескольких месяцев соблюдения рекомендаций мы заметили улучшение состояния.»
Игорь, 42 года, менеджер: «У меня паракератоз обнаружили случайно во время обследования. Я не понимал, что это такое. Врач объяснил, что это может быть признаком хронического гастрита или других заболеваний. Он рекомендовал мне изменить питание, начать заниматься спортом и следить за уровнем стресса. Честно говоря, это было непросто, но я старался придерживаться всем рекомендациям. Через пару месяцев явные симптомы исчезли, и я стал чувствовать себя лучше.»
Мария, 28 лет, студентка: «Когда я услышала от своего врача диагноз паракератоз, мне стало страшно. Я начала искать информацию в интернете и нашла много разных мнений. Врач успокоил меня, сказав, что это не смертельно, но требует внимания. Она назначила мне поддержку в виде витаминов и диетического питания. Сложнее всего было отказаться от сладкого, но ради здоровья я это сделала. Через время я заметила, что ощущения в пищеводе улучшились.»
Вопросы по теме
Как паракератоз пищевода влияет на пищеварение?
Паракератоз пищевода может вызывать нарушение нормального пищеварения, так как измененная структура клеток слизистой оболочки может снизить ее функциональность. Это приводит к появлению симптомов, таких как дискомфорт при глотании и изжога. Важно отметить, что паракератоз может быть связан с хроническими заболеваниями, такими как гастрит или рефлюкс, что требует комплексного подхода к диагностике и лечению.
Можно ли данный недуг предупредить, или он возникает неожиданно?
Предупредить появление паракератоза можно путем соблюдения определенных профилактических мер. К ним относятся полноценное питание, отказ от вредных привычек, таких как курение и чрезмерное употребление алкоголя, а также своевременное лечение заболеваний пищеварительного тракта. Однако в некоторых случаях паракератоз может развиваться в результате наследственной предрасположенности или в результате воздействия внешних факторов, что делает его возникновение менее предсказуемым.
Какова роль диеты при лечении паракератоза пищевода?
Диета играет ключевую роль в лечении паракератоза пищевода. Правильное питание может помочь уменьшить воспаление и улучшить общее состояние пищеварительной системы. Рекомендуется включать в рацион легкие, не раздражающие продукты, такие как отварные овощи, нежирные сорта мяса и молочные продукты. Избегание острого, кислого и сильно сладкого также поможет снизить симптомы и улучшить качество жизни пациента. В некоторых случаях может быть полезно проконсультироваться с диетологом для составления индивидуального плана питания.
